ORGANSKE KISIKOVE SPOJINE
|
|
|
- Vincenc Janežič
- pred 3 leti
- Pregledov:
Transkripcija
1 ORGANSKE KISIKOVE SPOJINE
2 VRSTE ORGANSKIH KISIKOVIH SPOJIN
3 Glavne funkcionalne skupine s kisikom
4
5 Organske kisikove spojine dietileter Eter
6 POIMENOVANJE ETROV etil metil eter dietil eter
7 Organske kisikove spojine Metanal ali formaldehid Aldehid
8 Naravni viri aldehidov Najdemo jih kot ključne sestavine mnogih eteričnih olj in začimb. Melisa Strukturna formula citrala Skeletna formula citrala Španski janež Strukturna formula propanala Skeletna formula
9 POIMENOVANJE ALDEHIDOV Končnica:»-al«
10
11 NALOGA Kolikšna masa metanala je v 12 mol tega aldehida? Poglobi svoje znanje v računanju.
12 Organske kisikove spojine Propanon ali aceton Keton
13 POIMENOVANJE KETONOV Končnica: on CH 3 CH 2 -CO-CH 2 -CH 2 -CH 3 heksan-3-on
14
15 Organske kisikove spojine Etil heptanoat Ester
16 ASPIRIN
17 Organske kisikove spojine Okusi in arome sadja in rož. Estri R-COO-R
18 Okus ali vonj Estri hruška pomaranča banana ananas jabolko jagoda
19 Ananas, banane in jagode vsebujejo ob drugih tudi značilni ester etilbutanoat, ki sadežem ob značilnem lastnem vonju prida svež saden vonj.
20 Cimet vonj estra etilcimamata Etilcimamat je ester cimetove kisline in alkohola etanola.
21 POIMENOVANJE ESTROV
22 metilpropanoat metilmetanoat propiletanoat
23 Organske kisikove spojine kis Karboksilna kislina
24 POIMENOVANJE KARBOKSILNIH KISLIN Končnica: ojska kislina HCOOH metanojska (mravljična) kislina CH 3 COOH etanojska (ocentna) kislina
25 Monokarboksilne kisline Dolžina C verige Strukturna formula Domače ime IUPAC poimenovanje C 1 H-COOH mravljična kislina metanojska k. C 2 CH 3 -COOH ocetna kislina etanojska kislina C 3 CH 3 -CH 2 -COOH propionska kislina propanojska kisl. C 4 CH 3 -(CH 2 ) 2 -COOH maslena kislina butanojska k. C 5 CH 3 -(CH 2 ) 3 -COOH valerianska kislina (baldrian) pentanojska k.
26
27 NALOGA: POIMENUJ SPOJINE
28 Organske kisikove spojine etanol Alkohol
29 FUNKCIONALNA SKUPINA: Končnica: -ol
30 Pri imenovanju višjih alkoholov pa moramo navajati položaj hidroksilne skupine. položajna izomera: se nanaša ne lego OH skupine
31 racionalna formula ime
32
33
34
35 Poznamo primarne Alkoholi alkohole, sekundarne in terciarne alkohole primarni alkohol sekundarni alkohol dva sosednja C-atoma etanol propan-2-ol terciarni alkohol tri sosednji C-atomi 2-metilpropan-2-ol
36 Poimenuj alkohole: CH 3 CH 2 OH CH 3 CH CH 2 OH CH 3 CH 3 CH CH 3 OH OH OH OH
37 POIMENUJ ALKOHOLE
38 Poimenuj alkohole:
39 Z racionalno formulo zapiši alkohole: metanol etanol etan-1,2-diol propan-1,2,3-triol ciklobutanol
40 ALKOHOLI
41 Uporaba etanola Alkoholi razkužilo za roke São Paulo, Brazil Z dodajanjem etanola bencinu tako zmanjšajo uvoz nafte. antiseptik
42 FIZIKALNE LASTNOSTI ALKOHOLOV
43 TOPNOST ALKOHOLOV Alkoholi imajo lastnosti polarnih kot nepolarnih molekul. Hidroksilna skupina predstavlja polarni del molekule, alkilna skupina (R-) pa nepolarnega. Fizikalne lastnosti alkohola so odvisne od velikosti polarnega in nepolarnega dela. polarni del nepolarni del
44 EKSPERIMENT: Topnost etanola v vodi in heksanu (cikloheksan, heptan) voda + etanol heksan + etanol heksan + voda
45 TOPNOST, VRELIŠČE ALKOHOLOV Ime IUPAC / Racionalna formula Vrelišče ( C) Topnost v vodi (g/l) Uporaba metanol CH 3 OH 65 neomejena gorivo, topilo etanol CH 3 CH 2 OH 78,5 neomejena alkoholne pijače, topilo propan-1-ol CH 3 CH 2 CH 2 OH 97,4 neomejena topilo butan-1-ol CH 3 CH 2 CH 2 CH 2 OH 117,2 7,9 topilo pentan-1-ol CH 3 CH 2 CH 2 CH 2 CH 2 OH 137,3 2,3 topilo
46 Prvi trije alkoholi (metanol, etanol in propan-1-ol) se mešajo z vodo v vseh razmerjih, torej so zelo dobro topni. Z naraščajočim številom ogljikovih atomov pa se topnost alkoholov v vodi manjša.
47 VRELIŠČA ALKOHOLOV IN ALKANOV Alkohol Ogljikovodi k Racionalna formula alkohola Racionalna formula ogljikovodika Vrelišče alkohola ( C) Vrelišče alkana ( C) metanol metan CH 3 OH CH etanol etan CH 3 CH 2 OH CH 3 CH 3 78,5 89 propan-1-ol butan-1-ol propan butan CH 3 CH 2 CH 2 OH CH 3 CH 2 CH 3 97,4 42 CH 3 CH 2 CH 2 CH 2 OH CH 3 CH 2 CH 2 CH 3 117,2 0,5 pentan-1-ol pentan CH 3 CH 2 CH 2 CH 2 CH 2 OH CH 3 CH 2 CH 2 CH 2 CH 3 137,3 36
48 VRELIŠČA ALKOHOLOV Alkoholi imajo VIŠJA vrelišča, kot alkani z enakim številom ogljikovih atomov. Alkoholi z daljšo verigo C atomov imajo višje vrelišče kot spojine s krajšo verigo C atomov.
49 ALKOHOLNO VRENJE ALI FERMENTACIJA Iz grozdnega soka pod vplivom gliv kvasovk poteče alkoholno vrenje. Pri vrenju iz sladkorja v grozdnem soku nastaneta etanol in ogljikov dioksid. C 6 H 12 O 6 2C 2 H 5 OH + 2CO 2
50 GORENJE ALKOHOLOV
51 GORENJE ALKOHOLOV Alkoholi so hlapne in vnetljive tekočine. Etanol gori z modrikastim plamenom in razpade na CO 2 in H 2 O. 2C 2 H 6 O(aq) + 6O 2 (g) 4CO 2 (g) + 6H 2 O(g)
52 EKSPERIMENT: Kako gorita etanol in heksan? OPAŽANJA: Plamenišče heksana ( 26 C), je nižje od plamenišča etanola (12 C), zato se hlapi heksana vžgejo hitreje. Etanol gori z nesvetečim plamenom. Heksan gori s svetečim plamenom.
53 REAKCIJE ALKOHOLOV
54 REAKCIJA Z NATRIJEM Reakcija natrija z alkoholom: Nastanejo SOLI
55 NASTANEK ETROV Eter nastane pri odcepu molekule vode iz dveh molekul alkohola. Reakcija poteka pri povišani temperaturi (180 ) in ob prisotnosti H 2 SO 4 kot katalizatorja.
56 OKSIDACIJA ALKOHOLOV Enicimi v jetrih oksidirajo ETANOL v ETANAL, tega v ETANOJSKO KISLINO, ki se pretvori v H 2 O in CO 2. Tako izločimo 90 % alkohola. Ostalo količino pa z znojenjem, urinom.
57 Enicimi v jetrih oksidirajo METANOL v METANAL, tega v METANOJSKO KISLINO, ki se pretvori v H 2 O in CO 2. METANAL ( formaldehid ) je hud strup, ki reagira z beljakovinami v očesu (slepota, strup) Formalin je tekočina za shranjevanje bioloških preparatov
58 OKSIDACIJA ALKOHOLOV Z oksidacijami alkoholov dobimo: aldehide, karboksilne kisline, ketone. Oksidanti: kalijev manganat (VII) (KMnO 4 ), kalijev dikromat (VI) (K 2 Cr 2 O 7 ),
59 A) OKSIDACIJA PRIMARNEGA ALKOHOLA nastajajo aldehidi, ki se ponavadi oksidirajo naprej do karboksilne kisline.
60 EKSPERIMENT: OKSIDACIJA ETANOLA OPAŽANJA: Kisla raztopina kalijevega dikromata, K 2 Cr 2 O 7, ki je oranžne barve, oksidira etanol do etanojske kisline, pri čemer se spremeni barva raztopine iz oranžne v zeleno.
61 2) OKSIDACIJA SEKUNDARNEGA ALKOHOLA nastajajo ketoni.
62 ELIMINACIJA VODE (DEHIDRIRANJE ETANOLA) Pri kemijski reakciji se iz ene same molekule odcepi molekula vode poteka pri povišani temperaturi (180 ) in ob prisotnosti H 2 SO 4 kot katalizatorja. nastane ALKEN C H 3 H C H H C OH H H 2 SO H 4 C C H + H OH 180 o C H 3 C H
63 NALOGA Izračunaj masni delež ogljika, vodika in kisika v molekuli etanola.
64 KARBOKSILNE KISLINE
65 Monokarboksilne kisline Dolžina C verige Strukturna formula Domače ime IUPAC poimenovanje C 1 H-COOH mravljična kislina metanojska k. C 2 CH 3 -COOH ocetna kislina etanojska kislina C 3 CH 3 -CH 2 -COOH propionska kislina propanojska kisl. C 4 CH 3 -(CH 2 ) 2 -COOH maslena kislina butanojska k. C 5 CH 3 -(CH 2 ) 3 -COOH valerianska kislina (baldrian) pentanojska k.
66 Formula / trivialno oz. udomačeno ime HCOOH mravljinčna kislina CH 3 COOH ocetna kislina CH 3 CH(OH)COOH mlečna kislina CH 3 CH 2 CH 2 COOH maslena kislina CH 3 CH 2 CH 2 CH 2 COOH valerijanska kislina CH 3 CH 2 CH 2 CH 2 CH 2 COOH kapronska kislina Ime po nomenklaturi IUPAC metanojska kislina etanojska kislina 2-hidroksipropanojska kislina butanojska kislina pentanojska kislina heksanojska kislina Vir tekočina v zadku mravelj kis kislo mleko, kislo zelje surovo maslo baldrijan surovo maslo, olje
67 EKSPERIMENT: ph raztopin karboksilnih kislin Snovi: ocetna kislina limonin sok citronska kislina jabolčni sok mleko pomarančni sok OPAŽANJA:
68 NALOGA Kolikšna masa etanojske kisline je v 25 mol te kisline?
69 JAKOST KARBOKSILNIH KISLIN Karboksilne kisline so šibke, le del molekul namreč reagira z vodo in tvori ione. Daljša kot je veriga ogljikovih atomov, tem šibkejše so. nepolarni del polarni del
70 Karboksilna skupina (COOH) je močno polarna, zato so nižje kisline (C 1 C 4 ) topne v vodi in tvorijo vodikovo vez. Posledično imajo VISOKA VRELIŠČA. spojina molska masa (g/mol) Tv ( C) butan 58 0,6 propanal propanol 60 ocetna kislina
71 Topnost karboksilnih kislin v vodi z dolžino verige pada.
72 VODNE RAZTOPINE KARBOKSILNIH KISLIN Karboksilne kisline reagirajo v vodi kot kisline. Pri reakciji z vodo tvorijo oksonijeve ione in karboksilatne anione. CH 3 COOH(aq) + H 2 O (l) CH 3 COO (aq) + H 3 O + (aq)
73 SOLI KARBOKSILNIH KISLIN Med raztopinami etanojske kisline in NaOH nastane vodna raztopina soli natrijevega acetata (etanoata). CH 3 COOH(aq) + NaOH(aq) CH 3 COONa(aq) + H 2 O(l)
74 NASTANEK ESTRA - estrenje: Alkoholi reagirajo s karboksilno kislino, odcepi se molekula vode in nastane ester. KATALIZATOR: močna kislina (H 2 SO 4 )
75 Dopolni reakcijo:
76 EKSPERIMENT: Po čem diši v kemijski učilnici? NALOGA: Ugotovi, kakšen je vonj produktov, nastalih pri segrevanju karboksilne kisline in alkohola.
77 POTEK DELA: 1. V epruveto daj 2 ml pentanola in 2 ml etanojske kisline. 2. Dodaj 2 do 3 kapljice koncentrirane žveplove kisline. 3. Epruveto previdno segrevaj, da zmes zavre. 4. Počakaj 30 sekund in dodaj 5 ml vodne raztopine natrijevega hidroksida. Vsebino epruvete previdno povohaj. Napiši opažanja.
78 ODGOVORI NA VPRAŠANJA: Zakaj je potrebno dodati žveplovo kislino v zmes alkohola in karboksilne kisline pred segrevanjem? Kaj nastane pri segrevanju alkohola in karboksilne kisline ob prisotnosti žveplove kisline? Napiši reakcijsko shemo nastanka produkta. Pri zapisu uporabi strukturne formule. Zapiši ime produkta. Po čem ima vonj?
79 EKSPERIMENT: Kako odpravimo neprijeten vonj?
80 Kaj se zgodi z vonjem kisline po dodatku baze? Napiši enačbo kemijske reakcije, ki poteče v prvi in drugi epruveti. Kako s skupnim imenom imenujemo snov, ki nastane v obeh epruvetah? Kakšen vonj ima ta snov v vodni raztopini?
IZBIRNI PREDMET KEMIJA 2. TEST B Ime in priimek: Število točk: /40,5t Ocena: 1.) 22,4 L kisika, merjenega pri 0 o C in 101,3 kpa: (1t) A im
 IZBIRNI PREDMET KEMIJA 2. TEST B Ime in priimek: 8. 1. 2008 Število točk: /40,5t Ocena: 1.) 22,4 L kisika, merjenega pri 0 o C in 101,3 kpa: (1t) A ima maso 16,0 g; B ima maso 32,0 g; C vsebuje 2,00 mol
IZBIRNI PREDMET KEMIJA 2. TEST B Ime in priimek: 8. 1. 2008 Število točk: /40,5t Ocena: 1.) 22,4 L kisika, merjenega pri 0 o C in 101,3 kpa: (1t) A ima maso 16,0 g; B ima maso 32,0 g; C vsebuje 2,00 mol
ALKOHOLI
 ALKOHOLI Kaj je alkohol? Alkohol je bistvena učinkovina v alkoholnih pijačah, ter alkoholi so pomembna skupina organskih spojin. V kemiji je alkohol splošen pojem, ki ga uporabljamo za vsako organsko spojino,
ALKOHOLI Kaj je alkohol? Alkohol je bistvena učinkovina v alkoholnih pijačah, ter alkoholi so pomembna skupina organskih spojin. V kemiji je alkohol splošen pojem, ki ga uporabljamo za vsako organsko spojino,
AMIN I
 AMI I Kaj so Amini Amini so zelo razširjene spojine v naravnih ali umetnih organskih snoveh.kemijsko so vezani v barvilih, zdravilih,alkaloidih in polimerih.prosti amini se redko pojavljajo v naravi, nastanejo
AMI I Kaj so Amini Amini so zelo razširjene spojine v naravnih ali umetnih organskih snoveh.kemijsko so vezani v barvilih, zdravilih,alkaloidih in polimerih.prosti amini se redko pojavljajo v naravi, nastanejo
10. Vaja: Kemijsko ravnotežje I a) Osnove: Poznamo enosmerne in ravnotežne kemijske reakcije. Za slednje lahko pišemo določeno konstanto kemijskega ra
 10. Vaja: Kemijsko ravnotežje I a) Osnove: Poznamo enosmerne in ravnotežne kemijske reakcije. Za slednje lahko pišemo določeno konstanto kemijskega ravnotežja (K C ), ki nam podaja konstantno razmerje
10. Vaja: Kemijsko ravnotežje I a) Osnove: Poznamo enosmerne in ravnotežne kemijske reakcije. Za slednje lahko pišemo določeno konstanto kemijskega ravnotežja (K C ), ki nam podaja konstantno razmerje
Microsoft Word - M doc
 Š i f r a k a n d i d a t a : ržavni izpitni center *M12143111* SPOMLNSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 7. junij 2012 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Š i f r a k a n d i d a t a : ržavni izpitni center *M12143111* SPOMLNSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 7. junij 2012 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Microsoft Word - M docx
 Š i f r a k a n d i d a t a : ržavni izpitni center *M18243121* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Sreda, 29. avgust 2018 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Š i f r a k a n d i d a t a : ržavni izpitni center *M18243121* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Sreda, 29. avgust 2018 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Microsoft PowerPoint vaja-salen
 Sinteza mimetika encima SD 1. stopnja: H 2 salen 18/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza N,N - bis(saliciliden)etilendiamina Predlagajte orositveni reagent za detekcijo poteka reakcije in za
Sinteza mimetika encima SD 1. stopnja: H 2 salen 18/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza N,N - bis(saliciliden)etilendiamina Predlagajte orositveni reagent za detekcijo poteka reakcije in za
Microsoft Word doc
 [ifra kandidata: r`avni izpitni center *M* PREPREZKUS KEMJ zpitna pola Marec / minut ovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik H ali plasti~no
[ifra kandidata: r`avni izpitni center *M* PREPREZKUS KEMJ zpitna pola Marec / minut ovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik H ali plasti~no
Microsoft Word doc
 [ifra kandidata: Dr `av ni iz pitni center *M* PREDPREZKUS KEMJA zpitna pola Marec / minut Dovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik B
[ifra kandidata: Dr `av ni iz pitni center *M* PREDPREZKUS KEMJA zpitna pola Marec / minut Dovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik B
DELOVANJE KATALIZATORJEV Cilji eksperimenta: Opazovanje delovanja encima katalaze, ki pospešuje razkroj vodikovega peroksida, primerjava njenega delov
 DELOVANJE KATALIZATORJEV Cilji eksperimenta: Opazovanje delovanja encima katalaze, ki pospešuje razkroj vodikovega peroksida, primerjava njenega delovanja z delovanjem nebeljakovinskih katalizatorjev in
DELOVANJE KATALIZATORJEV Cilji eksperimenta: Opazovanje delovanja encima katalaze, ki pospešuje razkroj vodikovega peroksida, primerjava njenega delovanja z delovanjem nebeljakovinskih katalizatorjev in
HALOGENI ELEMENTI
 HALOGENI ELEMENTI Halogeni elementi so elementi 7. skupine periodnega sistema elementov (ali VII. skupine). To so fluor, klor, brom in jod. Halogeni spadajo med nekovine. V elementarnem stanju obstajajo
HALOGENI ELEMENTI Halogeni elementi so elementi 7. skupine periodnega sistema elementov (ali VII. skupine). To so fluor, klor, brom in jod. Halogeni spadajo med nekovine. V elementarnem stanju obstajajo
Vsebina Energija pri gorenju notranja energija, entalpija, termokemijski račun, specifična toplota zgorevanja specifična požarna obremenitev
 Vsebina Energija pri gorenju notranja energija, entalpija, termokemijski račun, specifična toplota zgorevanja specifična požarna obremenitev P i entropija, prosta entalpija spontani procesi, gorenje pri
Vsebina Energija pri gorenju notranja energija, entalpija, termokemijski račun, specifična toplota zgorevanja specifična požarna obremenitev P i entropija, prosta entalpija spontani procesi, gorenje pri
PERIODNI SISTEM 1. skupina
 PERIODNI SISTEM 1. skupina OSNOVNA DEJSTVA & POJMI Vsi elementi so zelo reaktivni, zato jih hranimo pod pertolejem in vsi so mehke, srebrno bele kovine Vse spojine so ionske in topne Vsi elementi, oz.
PERIODNI SISTEM 1. skupina OSNOVNA DEJSTVA & POJMI Vsi elementi so zelo reaktivni, zato jih hranimo pod pertolejem in vsi so mehke, srebrno bele kovine Vse spojine so ionske in topne Vsi elementi, oz.
Uvod v OGRRANSKO KEMIJO / KEMIJO OGLKIKOVODIKOV in njihovih DERIVATOV Elementna sestava: SNOVI in SPOJINE Anorganske snovi vsi elementi (razen žlahtni
 Uvod v OGRRANSKO KEMIJO / KEMIJO OGLKIKOVODIKOV in njihovih DERIVATOV Elementna sestava: SNOVI in SPOJINE Anorganske snovi vsi elementi (razen žlahtnih plinov) Organske snovi C(ogljik),H(vodik),O(kisik),
Uvod v OGRRANSKO KEMIJO / KEMIJO OGLKIKOVODIKOV in njihovih DERIVATOV Elementna sestava: SNOVI in SPOJINE Anorganske snovi vsi elementi (razen žlahtnih plinov) Organske snovi C(ogljik),H(vodik),O(kisik),
1. Prehajanje snovi skozi celično membrano biološke membrane so izbirno prepustne (uravnavajo svojo kemijsko sestavo) membrana je o meja med celico oz
 1. Prehajanje snovi skozi celično membrano biološke membrane so izbirno prepustne (uravnavajo svojo kemijsko sestavo) membrana je o meja med celico oz. organeli in okoljem o regulator vstopa in izstopa
1. Prehajanje snovi skozi celično membrano biološke membrane so izbirno prepustne (uravnavajo svojo kemijsko sestavo) membrana je o meja med celico oz. organeli in okoljem o regulator vstopa in izstopa
MALICA oktober 2015 Preglednica učencev po razredih in število izpolnjenih anketnih vprašalnikov. Razred Učenci Št. odgovorov 4.a b a
 MALICA oktober 2015 Preglednica učencev po razredih in število izpolnjenih anketnih vprašalnikov. Razred Učenci odgovorov 4.a 20 20 4.b 19 18 5.a 2 22 6.a 17 17 6.b 17 17 7.a 14 1 7.b 16 15 8.a 20 20 8.b
MALICA oktober 2015 Preglednica učencev po razredih in število izpolnjenih anketnih vprašalnikov. Razred Učenci odgovorov 4.a 20 20 4.b 19 18 5.a 2 22 6.a 17 17 6.b 17 17 7.a 14 1 7.b 16 15 8.a 20 20 8.b
Slide 1
 Slide 1 OBDELAVA ODPADNE VODE Slide 2 KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE? KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE?! uravnavanje ph, alkalnosti! odstranjevanje ali dodajanje elementov!
Slide 1 OBDELAVA ODPADNE VODE Slide 2 KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE? KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE?! uravnavanje ph, alkalnosti! odstranjevanje ali dodajanje elementov!
Odgovori na vprašanja za anorgansko kemijo
 Odgovori na vprašanja za anorgansko kemijo 1. Zakon o stalnih masnih razmerjih Masno razmerje reagentov, v katerem se reagenti spajajo, je neodvisno od načina reakcije ter vedno isto. 2. Zakon o mnogokratnih
Odgovori na vprašanja za anorgansko kemijo 1. Zakon o stalnih masnih razmerjih Masno razmerje reagentov, v katerem se reagenti spajajo, je neodvisno od načina reakcije ter vedno isto. 2. Zakon o mnogokratnih
UREDBA KOMISIJE (EU) 2018/ z dne 28. septembra o spremembi Priloge II k Uredbi (ES) št. 1333/ Evropskega parlamen
 1.10.2018 L 245/1 II (Nezakonodajni akti) UREDBE UREDBA KOMISIJE (EU) 2018/1461 z dne 28. septembra 2018 o spremembi Priloge II k Uredbi (ES) št. 1333/2008 Evropskega parlamenta in Sveta ter Priloge k
1.10.2018 L 245/1 II (Nezakonodajni akti) UREDBE UREDBA KOMISIJE (EU) 2018/1461 z dne 28. septembra 2018 o spremembi Priloge II k Uredbi (ES) št. 1333/2008 Evropskega parlamenta in Sveta ter Priloge k
Analizna kemija I
 Analizna kemija I 2. Kemija raztopin Kaj je raztopina? Raztopina je zmes ionov ali molekul topljenca v topilu: Prave raztopine so homogene, raztopljeni (dispergirani) delci pa zelo majhni (ioni, molekule);
Analizna kemija I 2. Kemija raztopin Kaj je raztopina? Raztopina je zmes ionov ali molekul topljenca v topilu: Prave raztopine so homogene, raztopljeni (dispergirani) delci pa zelo majhni (ioni, molekule);
PROFILES učno gradivo, navodila za učitelje
 Se bom raztopil, če bo deževalo? Slika 1:diamanti (Vir: http://www.idb.it/; 18.10.2015) Slika 2: kristali kuhinjske soli (Vir: https://hr.wikipedia.org/wiki/kuhinjska _sol; 18.10.2015) Modul za poučevanje
Se bom raztopil, če bo deževalo? Slika 1:diamanti (Vir: http://www.idb.it/; 18.10.2015) Slika 2: kristali kuhinjske soli (Vir: https://hr.wikipedia.org/wiki/kuhinjska _sol; 18.10.2015) Modul za poučevanje
UVOD ČISTE SNOVI SNOV ločevanje mešanje ZMESI ELEMENT SPOJINE molekule (NaCl, ATOMI (He) MOLEKULE (F 2, Cl 2, Br 2, I 2, H 2, N 2, O 2, P 4, S 8 samo
 UVOD ČISTE SNOVI SNOV ločevanje mešanje ZMESI ELEMENT SPOJINE molekule (NaCl, ATOMI (He) MOLEKULE (F 2, Cl 2, Br 2, I 2, H 2, N 2, O 2, P 4, S 8 samo sobni pogoji!) AGREGATNA STANJA HOMOGENE zmes na pogled
UVOD ČISTE SNOVI SNOV ločevanje mešanje ZMESI ELEMENT SPOJINE molekule (NaCl, ATOMI (He) MOLEKULE (F 2, Cl 2, Br 2, I 2, H 2, N 2, O 2, P 4, S 8 samo sobni pogoji!) AGREGATNA STANJA HOMOGENE zmes na pogled
Microsoft Word - N doc
 Š i f r a u ~ e n c a: r`avni izpitni center *N072433* NKNNI ROK KEMIJ PREIZKUS ZNNJ Petek,. junija 2007 / 60 minut ovoljeno gradivo in pripomo~ki: u~enec prinese s seboj modro/~rno nalivno pero ali moder/~rn
Š i f r a u ~ e n c a: r`avni izpitni center *N072433* NKNNI ROK KEMIJ PREIZKUS ZNNJ Petek,. junija 2007 / 60 minut ovoljeno gradivo in pripomo~ki: u~enec prinese s seboj modro/~rno nalivno pero ali moder/~rn
Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim na
 Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim načrtom. Urejena je v osem poglavij (Varno eksperimentalno
Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim načrtom. Urejena je v osem poglavij (Varno eksperimentalno
Vpliv koncentracije etanola na delovanje gorivne celice
 Osnovna šola Hudinja Vpliv koncentracije etanola na delovanje gorivne celice raziskovalna naloga avtorice: Tjaša Hočevar, 9.b mentor: Boštjan Štih, prof. bio in kem Sara Skočir, 9.a Maruša Turnšek, 9.a
Osnovna šola Hudinja Vpliv koncentracije etanola na delovanje gorivne celice raziskovalna naloga avtorice: Tjaša Hočevar, 9.b mentor: Boštjan Štih, prof. bio in kem Sara Skočir, 9.a Maruša Turnšek, 9.a
Kako potekajo reakcije oksidacije in redukcije z manganati (VII) v nevtralni do zmerno alkalni raztopini
 VPRAŠANJA ZA ANALIZNO KEMIJO 1.) Kako potekajo reakcije oksidacije in redukcije z manganati(vii) v nevtralni do zmerno alkalni raztopini? Izberite si ustrezen reducent in napišite reakcijo! 2.) Kako reagirajo
VPRAŠANJA ZA ANALIZNO KEMIJO 1.) Kako potekajo reakcije oksidacije in redukcije z manganati(vii) v nevtralni do zmerno alkalni raztopini? Izberite si ustrezen reducent in napišite reakcijo! 2.) Kako reagirajo
GRADIVO ZA POSVETE
 MINISTRSTVO ZA OBRAMBO Uprava Republike Slovenije za zaščito in reševanje in GASILSKA ZVEZA SLOVENIJE MESEC VARSTVA PRED POŽAROM - GRADIVA - Ljubljana, september 2006 Opomba: Gradivo ni lektorirano in
MINISTRSTVO ZA OBRAMBO Uprava Republike Slovenije za zaščito in reševanje in GASILSKA ZVEZA SLOVENIJE MESEC VARSTVA PRED POŽAROM - GRADIVA - Ljubljana, september 2006 Opomba: Gradivo ni lektorirano in
Vsebina 5 Kaj moramo vedeti o mleku? Kemijska sestava mleka... 6 Kozje mleko Ovčje mleko Mikrobiološka naseljenost Postopki obdel
 Vsebina 5 Kaj moramo vedeti o mleku? Kemijska sestava mleka... 6 Kozje mleko... 10 Ovčje mleko... 11 Mikrobiološka naseljenost... 12 14 Postopki obdelave mleka v mlekarni Toplotna obdelava mleka... 16
Vsebina 5 Kaj moramo vedeti o mleku? Kemijska sestava mleka... 6 Kozje mleko... 10 Ovčje mleko... 11 Mikrobiološka naseljenost... 12 14 Postopki obdelave mleka v mlekarni Toplotna obdelava mleka... 16
JEDILNIK Zajtrk Kosilo Popoldanska malica Ponedeljek Torek Sreda Četrtek *mlečni gris iz pire v domačem mleku, čokoladni/cimetov posip, jagod
 Popoldanska malica 1.6.2017 *mlečni gris iz pire v domačem mleku, posip, jagode. goveja juha, pire krompir, kuhana eko govedina, kmečke kumare v smetanovi omaki marelični žepki, 100% pomarančni sok 2.6.2017
Popoldanska malica 1.6.2017 *mlečni gris iz pire v domačem mleku, posip, jagode. goveja juha, pire krompir, kuhana eko govedina, kmečke kumare v smetanovi omaki marelični žepki, 100% pomarančni sok 2.6.2017
1
 1. Pojme na desni poveži z ustreznimi spojinami in ioni na levi strani glede na njihove lastnosti in uporabo pri vaji določevanja glukoze in saharoze v skupnem vzorcu! Ni nujno, da si vsi pojmi povezani!
1. Pojme na desni poveži z ustreznimi spojinami in ioni na levi strani glede na njihove lastnosti in uporabo pri vaji določevanja glukoze in saharoze v skupnem vzorcu! Ni nujno, da si vsi pojmi povezani!
Tekmovanje iz naravoslovja Državno tekmovanje 25. januar 2014 Čas reševanja: 120 minut. Dovoljeni pripomočki: računalo, ravnilo, kotomer, šestilo, kem
 Tekmovanje iz naravoslovja Državno tekmovanje. januar 0 Čas reševanja: 0 minut. Dovoljeni pripomočki: računalo, ravnilo, kotomer, šestilo, kemični svinčnik, svinčnik, radirka. Periodni sistem je na zadnji
Tekmovanje iz naravoslovja Državno tekmovanje. januar 0 Čas reševanja: 0 minut. Dovoljeni pripomočki: računalo, ravnilo, kotomer, šestilo, kemični svinčnik, svinčnik, radirka. Periodni sistem je na zadnji
Microsoft Word - Conditioner for Leather 86 SDS SVN V2.doc
 Varnostni List BALZAM ZA USNJE ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: BALZAM ZA USNJE Koda izdelka: 86 1.2. Pomembne identificirane uporabe snovi ali zmesi
Varnostni List BALZAM ZA USNJE ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: BALZAM ZA USNJE Koda izdelka: 86 1.2. Pomembne identificirane uporabe snovi ali zmesi
JEDILNIK OD IN SLAŠČIČARSKI IZDELKI (ŽEMLJE,PECIVO, PIŠKOTI )LAHKO VSEBUJEJO POLEG GLUTENA TUDI SLEDI MLEČNIH IN SOJINIH BELJAKOVIN
 OD 1.9.2016 IN 2.9.2016 SLAŠČIČARSKI IZDELKI (ŽEMLJE,PECIVO, PIŠKOTI )LAHKO VSEBUJEJO POLEG GLUTENA TUDI SLEDI MLEČNIH IN SOJINIH BELJAKOVIN TER SLEDI OREŠKOV IN SEZAMA! ZLATE MISLI O POGUMU: Naša pot
OD 1.9.2016 IN 2.9.2016 SLAŠČIČARSKI IZDELKI (ŽEMLJE,PECIVO, PIŠKOTI )LAHKO VSEBUJEJO POLEG GLUTENA TUDI SLEDI MLEČNIH IN SOJINIH BELJAKOVIN TER SLEDI OREŠKOV IN SEZAMA! ZLATE MISLI O POGUMU: Naša pot
JEDILNIK SEPTEMBER 2004
 1.8.2019 ajdov kruh meden namaz (čebelarstvo Ivan Bračko) rezine melone rezine šunke /rezine sira rezine svežega paradižnika z bučnim oljem brokoli kremna juha lazanja z govedino kumarična solata s čebulo
1.8.2019 ajdov kruh meden namaz (čebelarstvo Ivan Bračko) rezine melone rezine šunke /rezine sira rezine svežega paradižnika z bučnim oljem brokoli kremna juha lazanja z govedino kumarična solata s čebulo
VARNOSTNI LIST
 MEGLIO WC DEO Bouquet Varnostni list 1. IDENTIFIKACIJA SNOVI/PRIPRAVKA IN PODATKI O DOBAVITELJU 1.1. Identifikacija snovi ali pripravka: MEGLIO WC DEO Bouquet. 1.2. Podatki o dobavitelju: ARONA TRGOVINA
MEGLIO WC DEO Bouquet Varnostni list 1. IDENTIFIKACIJA SNOVI/PRIPRAVKA IN PODATKI O DOBAVITELJU 1.1. Identifikacija snovi ali pripravka: MEGLIO WC DEO Bouquet. 1.2. Podatki o dobavitelju: ARONA TRGOVINA
Microsoft Word - PARKETOLIT 1554A SL.doc
 Datum zadnje revidirane izdaje: 14.01.2013 Zamenjuje izdajo: / VARNOSTNI LIST 1. IDENTIFIKACIJA SNOVI / PRIPRAVKA IN DRUŽBE / PODJETJA: Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka:
Datum zadnje revidirane izdaje: 14.01.2013 Zamenjuje izdajo: / VARNOSTNI LIST 1. IDENTIFIKACIJA SNOVI / PRIPRAVKA IN DRUŽBE / PODJETJA: Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka:
1
 1. Izpit: 23.04.1992 1. Skiciraj strukture skupin NO 2+, NO 2, NO 2-! Pripiši sledeče kote O-N-O in razdalje N- O posamezne strukture: Koti: 115,4 o, 180 o in 134,4 o Razdalje:1,20, 1,15 in 1,24 0 A 2.
1. Izpit: 23.04.1992 1. Skiciraj strukture skupin NO 2+, NO 2, NO 2-! Pripiši sledeče kote O-N-O in razdalje N- O posamezne strukture: Koti: 115,4 o, 180 o in 134,4 o Razdalje:1,20, 1,15 in 1,24 0 A 2.
DATUM
 DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša (gluten, - obara z mesom, jagodni cmok (gluten, kivi, polžek (gluten, soja, 29. 4. 2019 soja, mleko, jajca,, polbel kruh (gluten, soja,
DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša (gluten, - obara z mesom, jagodni cmok (gluten, kivi, polžek (gluten, soja, 29. 4. 2019 soja, mleko, jajca,, polbel kruh (gluten, soja,
UNIVERZA V MARIBORU PEDAGOŠKA FAKULTETA RAZREDNI POUK ŽIVA BITJA VSEBUJEJO VODO (vaja pri predmetu Didaktični praktikum iz biologije in kemije) Ime in
 UNIVERZA V MARIBORU PEDAGOŠKA FAKULTETA RAZREDNI POUK ŽIVA BITJA VSEBUJEJO VODO (vaja pri predmetu Didaktični praktikum iz biologije in kemije) Ime in priimek: D. V. Skupina: 5 / D Maribor, 7. 5. 2012
UNIVERZA V MARIBORU PEDAGOŠKA FAKULTETA RAZREDNI POUK ŽIVA BITJA VSEBUJEJO VODO (vaja pri predmetu Didaktični praktikum iz biologije in kemije) Ime in priimek: D. V. Skupina: 5 / D Maribor, 7. 5. 2012
PowerPoint Presentation
 Tehnološki izzivi proizvodnja biometana in njegovo injiciranje v plinovodno omrežje prof. dr. Iztok Golobič Predstojnik Katedre za toplotno in procesno tehniko Vodja Laboratorija za toplotno tehniko Fakulteta
Tehnološki izzivi proizvodnja biometana in njegovo injiciranje v plinovodno omrežje prof. dr. Iztok Golobič Predstojnik Katedre za toplotno in procesno tehniko Vodja Laboratorija za toplotno tehniko Fakulteta
PONEDELJEK OD IN MALICA ŠTRUČKA S HRENOVKO, 100% JABOLČNI SOK KOSILO CVETAČNA JUHA, MESNO ZELENJAVNA RIŽOTA, SOLATA ALERGENI GLUT
 OD 06. 11. IN 10. 11. 2017 ŠTRUČKA S HRENOVKO, 100% JABOLČNI SOK CVETAČNA JUHA, MESNO ZELENJAVNA RIŽOTA, ALERGENI GLUTEN MLEKO, GLUTEN, JAJCA, ZELENA KROMPIRJEV KRUH, ČOKOLADNI NAMAZ, KISLA SMETANA, BELA
OD 06. 11. IN 10. 11. 2017 ŠTRUČKA S HRENOVKO, 100% JABOLČNI SOK CVETAČNA JUHA, MESNO ZELENJAVNA RIŽOTA, ALERGENI GLUTEN MLEKO, GLUTEN, JAJCA, ZELENA KROMPIRJEV KRUH, ČOKOLADNI NAMAZ, KISLA SMETANA, BELA
PowerPointova predstavitev
 CATERING MARIPOSA CATERING SPECIALTY COFFEE KAJ POČNEMO Posebnost kavnega cateringa je v tem, da prinaša vašemu dogodku brezkompromisno najvišjo kakovost. Naši prenosni espresso bar dovoljuje našim profesionalnim
CATERING MARIPOSA CATERING SPECIALTY COFFEE KAJ POČNEMO Posebnost kavnega cateringa je v tem, da prinaša vašemu dogodku brezkompromisno najvišjo kakovost. Naši prenosni espresso bar dovoljuje našim profesionalnim
«Naziv_PP»
 POMURSKI SEJEM d.d., Gornja Radgona MEDNARODNO OCENJEVANJE SADNIH SOKOV, PIJAČ IN EMBALIRANIH VOD 2016 Rezultati ocenjevanja po podjetjih ARC-Kranj, d.o.o. Hrastje 52k, SI-4000 Kranj Telefon: 04/292 7600
POMURSKI SEJEM d.d., Gornja Radgona MEDNARODNO OCENJEVANJE SADNIH SOKOV, PIJAČ IN EMBALIRANIH VOD 2016 Rezultati ocenjevanja po podjetjih ARC-Kranj, d.o.o. Hrastje 52k, SI-4000 Kranj Telefon: 04/292 7600
JEDILNIK SEPTEMBER 2004
 1.7.2019 rahli ovseni kosmiči na nehomogenizirano mleko / rezine temnega kruha rezine banane piščančji paprikaš s svežo papriko koruzna polenta solata iz mladega zelja ½ sezamove štručke 2.7.2019 ovsen
1.7.2019 rahli ovseni kosmiči na nehomogenizirano mleko / rezine temnega kruha rezine banane piščančji paprikaš s svežo papriko koruzna polenta solata iz mladega zelja ½ sezamove štručke 2.7.2019 ovsen
PRILOGA II OSNOVNA SESTAVA NADALJEVALNIH FORMUL ZA DOJENČKE IN MAJHNE OTROKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti, določene v Prilogi, s
 PRILOGA II OSNOVNA SESTAVA NADALJEVALNIH FORMUL ZA DOJENČKE IN MAJHNE OTROKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti, določene v Prilogi, se nanašajo na končno pripravljeni obrok, ki se kot
PRILOGA II OSNOVNA SESTAVA NADALJEVALNIH FORMUL ZA DOJENČKE IN MAJHNE OTROKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti, določene v Prilogi, se nanašajo na končno pripravljeni obrok, ki se kot
JEDILNIK: let OBROKI PONEDELJEK, TOREK, SREDA, ČETRTEK, PETEK, Zajtrk Bel kruh, maslo, Pirin kr
 JEDILNIK: 31. 12. 4. 1. 2019 OBROKI PONEDELJEK, 31. 12. TOREK, 1. 1. SREDA, 2. 1. ČETRTEK, 3. 1. PETEK, 4. 1. Zajtrk Bel kruh, maslo, Pirin kruh, pašteta argeta, kislo Mlečni zdrob s kakavovim marmelada,
JEDILNIK: 31. 12. 4. 1. 2019 OBROKI PONEDELJEK, 31. 12. TOREK, 1. 1. SREDA, 2. 1. ČETRTEK, 3. 1. PETEK, 4. 1. Zajtrk Bel kruh, maslo, Pirin kruh, pašteta argeta, kislo Mlečni zdrob s kakavovim marmelada,
PETEK ČETRTEK SREDA TOREK PONEDELJEK VRTEC HRASTNIK 1430 Hrastnik, Novi log 11A Tel: ZA 1. IN 2. STAROSTNO OBDOBJE DAN ZAJTRK KOSILO POP.
 BUHTELJ, KAKAV iz mleka lokalnega izvora ZELENJAVNA JUHA, ZAPEČENE TESTENINE S ŠUNKO, ZELENA SOLATA Z RADIČEM PREPEČENEC,* KRUH POLBELI KRUH, KUHAN PRŠUT, KISLA KUMARICA, BROKOLIJEVA KREMNA JUHA Z ZVEZDICAMI,
BUHTELJ, KAKAV iz mleka lokalnega izvora ZELENJAVNA JUHA, ZAPEČENE TESTENINE S ŠUNKO, ZELENA SOLATA Z RADIČEM PREPEČENEC,* KRUH POLBELI KRUH, KUHAN PRŠUT, KISLA KUMARICA, BROKOLIJEVA KREMNA JUHA Z ZVEZDICAMI,
PREPREČEVANJE DEHIDRACIJE Datum: Avtor: Klemen Vidmar Razred: 1.A Mentor: prof. Klemen Gutman Prof. Helena Črne Hladnik
 PREPREČEVANJE DEHIDRACIJE Datum: 6.6.13 Avtor: Klemen Vidmar Razred: 1.A Mentor: prof. Klemen Gutman Prof. Helena Črne Hladnik Kazalo 1. Uvod...3 2. Fizikalne in kemijske lastnosti vode (vodikove vezi)....3,4
PREPREČEVANJE DEHIDRACIJE Datum: 6.6.13 Avtor: Klemen Vidmar Razred: 1.A Mentor: prof. Klemen Gutman Prof. Helena Črne Hladnik Kazalo 1. Uvod...3 2. Fizikalne in kemijske lastnosti vode (vodikove vezi)....3,4
JEDILNIK: OBROKI PONEDELJEK, TOREK, SREDA, ČETRTEK, PETEK, Zajtrk Dop. malica SREČNO 2018! Samopostre
 JEDILNIK: 3. 1. 4. 1. 2019 OBROKI PONEDELJEK, 31. 12. TOREK, 1. 1. SREDA, 2. 1. ČETRTEK, 3. 1. PETEK, 4. 1. SREČNO 2018! Samopostrežni zajtrk:sadje, koruzni kosmiči, namaz (med, marmelada, maslo, smetanov
JEDILNIK: 3. 1. 4. 1. 2019 OBROKI PONEDELJEK, 31. 12. TOREK, 1. 1. SREDA, 2. 1. ČETRTEK, 3. 1. PETEK, 4. 1. SREČNO 2018! Samopostrežni zajtrk:sadje, koruzni kosmiči, namaz (med, marmelada, maslo, smetanov
JEDILNIK Dan Zajtrk Dopoldanska malica Kosilo Popoldanska malica Ponedeljek Mleko/ laktoza Čokolino/ čokoladne kroglice/ mus
 JEDILNIK 22.1. Dan Zajtrk Dopoldanska malica Kosilo Popoldanska malica Mleko/ laktoza Čokolino/ čokoladne kroglice/ mussli /gluten Sirova štručka/ laktoza, gluten Mortadela/gorčično seme Brokolijeva kremna
JEDILNIK 22.1. Dan Zajtrk Dopoldanska malica Kosilo Popoldanska malica Mleko/ laktoza Čokolino/ čokoladne kroglice/ mussli /gluten Sirova štručka/ laktoza, gluten Mortadela/gorčično seme Brokolijeva kremna
OSNOVNA ŠOLA RADA ROBIČA LIMBUŠ
 1. TEDEN od 31. 12. - 4. 1. 19 31. 12. 2019 1. 1. 2019 2. 1. 2019 3. 1. 2019 4. 1. 2019 LETNE POČITNICE Koruzni kruh, različni namazi, otroški Čokolešnik, mleko LETNE POČITNICE Mlečni kruh, tamar namaz,
1. TEDEN od 31. 12. - 4. 1. 19 31. 12. 2019 1. 1. 2019 2. 1. 2019 3. 1. 2019 4. 1. 2019 LETNE POČITNICE Koruzni kruh, različni namazi, otroški Čokolešnik, mleko LETNE POČITNICE Mlečni kruh, tamar namaz,
PREIZKUS ZNANJA BIOLOGIJA 8.a razred
 JEDILNIK 17. 4. 21. 4. 2017 MALICA MALICA ZA PODALJŠANO BIVANJE po 15.uri 17. 4. 18. 4. PAŠTETA, BELI KRUH, PAPRIKA, ČAJ, JABOLKO JUHA Z REZANCI, MAKARONOVO MESO, KUMARICE S PARADIŽNIKOM V SOLATI SENDVIČ,
JEDILNIK 17. 4. 21. 4. 2017 MALICA MALICA ZA PODALJŠANO BIVANJE po 15.uri 17. 4. 18. 4. PAŠTETA, BELI KRUH, PAPRIKA, ČAJ, JABOLKO JUHA Z REZANCI, MAKARONOVO MESO, KUMARICE S PARADIŽNIKOM V SOLATI SENDVIČ,
PRILOGA I PARAMETRI IN MEJNE VREDNOSTI PARAMETROV Splošne zahteve za pitno vodo DEL A Mikrobiološki parametri Parameter Mejna vrednost parametra (štev
 PRILOGA I PARAMETRI IN MEJNE VREDNOSTI PARAMETROV Splošne zahteve za pitno vodo DEL A Mikrobiološki parametri (število/100 ml) Escherichia coli (E. coli) 0 Enterokoki 0 Zahteve za vodo, namenjeno za pakiranje:
PRILOGA I PARAMETRI IN MEJNE VREDNOSTI PARAMETROV Splošne zahteve za pitno vodo DEL A Mikrobiološki parametri (število/100 ml) Escherichia coli (E. coli) 0 Enterokoki 0 Zahteve za vodo, namenjeno za pakiranje:
Microsoft Word - poprava diplome_03_10_2016.doc
 Diplomsko delo OBDELAVA ODPADNIH VOD IZ PROIZVODNJE 5-NOK (5-NITRO-8-HIDROKSIKINOLIN) Maribor, september 216 Kristjan Grobin Kristjan Grobin (5-nitro-8-hidroksikinolin) Diplomsko delo Maribor, 216 (5-nitro-8-hidroksikinolin)
Diplomsko delo OBDELAVA ODPADNIH VOD IZ PROIZVODNJE 5-NOK (5-NITRO-8-HIDROKSIKINOLIN) Maribor, september 216 Kristjan Grobin Kristjan Grobin (5-nitro-8-hidroksikinolin) Diplomsko delo Maribor, 216 (5-nitro-8-hidroksikinolin)
PRILOGA I OSNOVNA SESTAVA ZAČETNIH FORMUL ZA DOJENČKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti določene v tej prilogi se nanašajo na končno
 PRILOGA I OSNOVNA SESTAVA ZAČETNIH FORMUL ZA DOJENČKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti določene v tej prilogi se nanašajo na končno pripravljeni obrok, ki se kot tak daje v promet ali
PRILOGA I OSNOVNA SESTAVA ZAČETNIH FORMUL ZA DOJENČKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti določene v tej prilogi se nanašajo na končno pripravljeni obrok, ki se kot tak daje v promet ali
Microsoft PowerPoint - ep-vaja-02-web.pptx
 Goriva, zrak, dimni plini gorivo trdno, kapljevito: C, H, S, O, N, H 2 O, pepel plinasto: H 2, C x H y, CO 2, N 2,... + zrak N 2, O 2, (H 2 O, CO 2, Ar,...) dimni plini N 2, O 2, H 2 O, CO 2, SO 2 + toplota
Goriva, zrak, dimni plini gorivo trdno, kapljevito: C, H, S, O, N, H 2 O, pepel plinasto: H 2, C x H y, CO 2, N 2,... + zrak N 2, O 2, (H 2 O, CO 2, Ar,...) dimni plini N 2, O 2, H 2 O, CO 2, SO 2 + toplota
MATEMATIKA – IZPITNA POLA 1 – OSNOVNA IN VIŠJA RAVEN
 Državni izpitni center *M18242123* JESENSKI IZPITNI ROK BIOLOGIJA NAVODILA ZA OCENJEVANJE Četrtek, 30. avgust 2018 SPLOŠNA MATURA Državni izpitni center Vse pravice pridržane. M182-421-2-3 2 Naloga Odgovor
Državni izpitni center *M18242123* JESENSKI IZPITNI ROK BIOLOGIJA NAVODILA ZA OCENJEVANJE Četrtek, 30. avgust 2018 SPLOŠNA MATURA Državni izpitni center Vse pravice pridržane. M182-421-2-3 2 Naloga Odgovor
Zajtrk Ponedeljek Torek Sreda kruh s semeni, kisla smetana, džem, sadni čaj Šolska malica PRAZNIK PRAZNIK pletena štr
 1. 1. 2018 2. 1. 2018 3. 1. 2018 kruh s semeni, kisla smetana, džem, sadni PRAZNIK PRAZNIK pletena štručka, napitek, mleko (SŠH) 4. 1. 2018 ajdovi žganci, mleko, ocvirki polbeli kruh, hrenovka, ajvar,
1. 1. 2018 2. 1. 2018 3. 1. 2018 kruh s semeni, kisla smetana, džem, sadni PRAZNIK PRAZNIK pletena štručka, napitek, mleko (SŠH) 4. 1. 2018 ajdovi žganci, mleko, ocvirki polbeli kruh, hrenovka, ajvar,
DATUM
 DATUM ZAJTRK KOSILO POPOLDANSKA ribji namaz (ribe), ržen - zelenjavna enolončnica, palačinke brez rženi kruh (gluten, soja, 30. 10. 2017 kruh (gluten, soja, sezam), otroški čaj, mandarina laktoze (gluten,
DATUM ZAJTRK KOSILO POPOLDANSKA ribji namaz (ribe), ržen - zelenjavna enolončnica, palačinke brez rženi kruh (gluten, soja, 30. 10. 2017 kruh (gluten, soja, sezam), otroški čaj, mandarina laktoze (gluten,
VARNOSTNI LIST dir. EU 1907/2006; usklajeno z Prilogo 1 uredba 453/ / 9 BLESK -30C ZIMSKO ČISTILO VETROBRANSKIH STEKEL Verzija št:1 Datum izdaje
 VARNOSTNI LIST dir. EU 1907/2006; usklajeno z Prilogo 1 uredba 453/2010 1 / 9 Verzija št:1 1. IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1 Identifikator izdelka Proizvod BLESK -30C - ZIMSKO ČISTILO
VARNOSTNI LIST dir. EU 1907/2006; usklajeno z Prilogo 1 uredba 453/2010 1 / 9 Verzija št:1 1. IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1 Identifikator izdelka Proizvod BLESK -30C - ZIMSKO ČISTILO
DATUM
 DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša nesladka - obara z mesom, ajdova palačinka (gluten, kivi, polnoznata štručka 29. 4. 2019 (gluten, soja, mleko, jajca,, polbel kruh (gluten,
DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša nesladka - obara z mesom, ajdova palačinka (gluten, kivi, polnoznata štručka 29. 4. 2019 (gluten, soja, mleko, jajca,, polbel kruh (gluten,
Gorivna celica
 Laboratorij za termoenergetiko Delovanje gorivnih celic Najbolj uveljavljeni tipi gorivnih celic Obstaja veliko različnih vrst gorivnih celic, najpogosteje se jih razvršča glede na vrsto elektrolita Obratovalna
Laboratorij za termoenergetiko Delovanje gorivnih celic Najbolj uveljavljeni tipi gorivnih celic Obstaja veliko različnih vrst gorivnih celic, najpogosteje se jih razvršča glede na vrsto elektrolita Obratovalna
OSNOVNA ŠOLA RADA ROBIČA LIMBUŠ
 1. TEDEN od 30. 4. - 4. 5. 18 30. 4. 2018 1. 5. 2018 2. 5. 2018 3. 5. 2018 4. 5. 2018 Turist kruh, umešana jajčka, otroški čaj Štručka z zeliščnim maslom, kakav z domačim mlekom Makaronovo meso z zelenjavo,
1. TEDEN od 30. 4. - 4. 5. 18 30. 4. 2018 1. 5. 2018 2. 5. 2018 3. 5. 2018 4. 5. 2018 Turist kruh, umešana jajčka, otroški čaj Štručka z zeliščnim maslom, kakav z domačim mlekom Makaronovo meso z zelenjavo,
OSNOVNA ŠOLA
 1. TEDEN od 6. 11. 10. 11. 2017 6. 11. 2017 7. 11. 2017 Čokolešnik, Koruzna žemlja, trdo kuhano jajce, zelena paprika, Pica, juice (malica po izboru 5. c-razreda) Ludvikov lonec, kruh, jabolčni zavitek
1. TEDEN od 6. 11. 10. 11. 2017 6. 11. 2017 7. 11. 2017 Čokolešnik, Koruzna žemlja, trdo kuhano jajce, zelena paprika, Pica, juice (malica po izboru 5. c-razreda) Ludvikov lonec, kruh, jabolčni zavitek
JEDILNIK ZA TEDEN VRTEC ZAJTRK MALICA KOSILO MALICA PONEDELJEK Črn kruh, ribji namaz, svež paradižnik, sadje sadje Zelenjavna j
 1. 8. 5. 8. 2016 1. 8. ribji namaz, svež paradižnik, Zelenjavna juha z rižkom, telečji zrezek v omaki, kuskus, zelnata solata s korenčkom Polnozrnati grisini, sadni 2. 8. Žganci,, Goveja juha z rezanci,
1. 8. 5. 8. 2016 1. 8. ribji namaz, svež paradižnik, Zelenjavna juha z rižkom, telečji zrezek v omaki, kuskus, zelnata solata s korenčkom Polnozrnati grisini, sadni 2. 8. Žganci,, Goveja juha z rezanci,
FIZIKALNA STANJA IN UREJENOST POLIMERNIH VERIG Polimeri se od nizkomolekularnih spojin razlikujejo po naravi fizikalnega stanja in po morfologiji. Gle
 FIZIKALNA STANJA IN UREJENOST POLIMERNIH VERIG Polimeri se od nizkomolekularnih spojin razlikujejo po naravi fizikalnega stanja in po morfologiji. Glede na obliko in način urejanja polimernih verig v trdnem
FIZIKALNA STANJA IN UREJENOST POLIMERNIH VERIG Polimeri se od nizkomolekularnih spojin razlikujejo po naravi fizikalnega stanja in po morfologiji. Glede na obliko in način urejanja polimernih verig v trdnem
DATUM
 DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša nesladka - obara s kunčjim mesom, ajdova palačinka kivi, polnoznata štručka 30. 4. 2018 (gluten, soja, mleko, jajca,, polbel kruh (gluten,
DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša nesladka - obara s kunčjim mesom, ajdova palačinka kivi, polnoznata štručka 30. 4. 2018 (gluten, soja, mleko, jajca,, polbel kruh (gluten,
Osnove gastronomije PREBAVA MAKROHRANIL IN Vpliv senzoričnih lastnosti na prebavo Barbara HERLAH, univ. dipl. inž. živ. teh.
 Osnove gastronomije PREBAVA MAKROHRANIL IN Vpliv senzoričnih lastnosti na prebavo Barbara HERLAH, univ. dipl. inž. živ. teh. PREBAVA (DIGESTIJA) IN VSRKAVANJE (ABSORPCIJA) V PREBAVILIH OH, B in M so uporabni
Osnove gastronomije PREBAVA MAKROHRANIL IN Vpliv senzoričnih lastnosti na prebavo Barbara HERLAH, univ. dipl. inž. živ. teh. PREBAVA (DIGESTIJA) IN VSRKAVANJE (ABSORPCIJA) V PREBAVILIH OH, B in M so uporabni
Izpit kemiki 23
 Izpit kemiki 23.4.1992 1.) Skiciraj strukture skupin NO 2+, NO 2-, NO 2. Pripiši sledeče kote O-N-O in razdalje N-O posamezne strukture: koti: 115,4, 180 in 134,3 razdalje: 1,20, 1,15 in 1,24Å 2.) Pri
Izpit kemiki 23.4.1992 1.) Skiciraj strukture skupin NO 2+, NO 2-, NO 2. Pripiši sledeče kote O-N-O in razdalje N-O posamezne strukture: koti: 115,4, 180 in 134,3 razdalje: 1,20, 1,15 in 1,24Å 2.) Pri
O S N O V N A Š O L A C I R K O V C E,Cirkovce 47, 2326 Cirkovce, DŠ: Telefon: (02) , telefaks: (02) ,
 PONEDELJEK, 5. 11. 2018 MALICA Mlečna juha(1,4),banana, čaj Piščančja obara z žličniki(1,2,3,8), rženi kruh(1,2,3), palačinke z marmelado(1,2,3) TOREK, 6. 11. 2018 MALICA Francoski rogljiček(1,2,3,4),
PONEDELJEK, 5. 11. 2018 MALICA Mlečna juha(1,4),banana, čaj Piščančja obara z žličniki(1,2,3,8), rženi kruh(1,2,3), palačinke z marmelado(1,2,3) TOREK, 6. 11. 2018 MALICA Francoski rogljiček(1,2,3,4),
DATUM
 DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša (gluten, - obara brez jajc z mesom, jagodni cmok kivi, polžek brez jajc 29. 4. 2019 soja, mleko, jajca, sezam), polbel kruh (gluten, soja,,
DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA mlečna prosena kaša (gluten, - obara brez jajc z mesom, jagodni cmok kivi, polžek brez jajc 29. 4. 2019 soja, mleko, jajca, sezam), polbel kruh (gluten, soja,,
OŠ FLV Slivnica pri Mariboru Vrtec Slivnica Mariborska cesta Orehova vas OBROK DATUM PONEDELJEK TOREK SREDA ČETRTEK
 5. 12. 6. 12. 7. 12. 8. 12. KAMILIČNI ČAJ AJDOV KRUH 1 TRDI SIR NARIBAN KORENČEK MLEKO (KMETIJA FREŠER)7 MLEČNI PARKELJ 1 OTROŠKI ČAJ HOT DOG ŠTRUČKA 1 HRENOVKA, GORČICA MLEČNI RIBANCI S ČOKOLADNIM POSIPOM
5. 12. 6. 12. 7. 12. 8. 12. KAMILIČNI ČAJ AJDOV KRUH 1 TRDI SIR NARIBAN KORENČEK MLEKO (KMETIJA FREŠER)7 MLEČNI PARKELJ 1 OTROŠKI ČAJ HOT DOG ŠTRUČKA 1 HRENOVKA, GORČICA MLEČNI RIBANCI S ČOKOLADNIM POSIPOM
Kmetijska šola Grm Sevno Novo mesto PROIZVODNJA IN UPORABA ENCIMOV Marec, 2007
 Kmetijska šola Grm Sevno 13 8000 Novo mesto PROIZVODNJA IN UPORABA ENCIMOV Marec, 2007 O ENCIMIH So najpomembnejša skupina beljakovin, so biokatalizatorji, znanih je okoli 3000, znižujejo aktivacijsko
Kmetijska šola Grm Sevno 13 8000 Novo mesto PROIZVODNJA IN UPORABA ENCIMOV Marec, 2007 O ENCIMIH So najpomembnejša skupina beljakovin, so biokatalizatorji, znanih je okoli 3000, znižujejo aktivacijsko
Osnovna šola Gabrovka - Dole
 Jedilnik za 49. teden od 1. avgusta do 5. avgusta 2011 1.8. topljeni sir planinski čaj z limono krompirjev golaž čokoladni puding s smetano polnozrnati piškoti nektarina 2.8. sadni musli navadni jogurt
Jedilnik za 49. teden od 1. avgusta do 5. avgusta 2011 1.8. topljeni sir planinski čaj z limono krompirjev golaž čokoladni puding s smetano polnozrnati piškoti nektarina 2.8. sadni musli navadni jogurt
Ljubljana,11
 DIETNI JEDILNIK ZA OTROKE 1. STAROSTNEGA OBDOBJA - DIETA brez mleka, jajc, soje, arašidov in oreščkov, jagod, sezama, (vzg. Vida, E. Mo) MOJCA/VJ ZA OBDOBJE OD 15.06. DO 19.06.2015 Bio pšenični kruh* (B-forma),
DIETNI JEDILNIK ZA OTROKE 1. STAROSTNEGA OBDOBJA - DIETA brez mleka, jajc, soje, arašidov in oreščkov, jagod, sezama, (vzg. Vida, E. Mo) MOJCA/VJ ZA OBDOBJE OD 15.06. DO 19.06.2015 Bio pšenični kruh* (B-forma),
PRIDOBIVANJE ELEKTRIČNE ENERGIJE Z GORIVNO CELICO
 Mestna občina Celje, Mladi za Celje Pridobivanje električne energije z gorivno celico Raziskovalna naloga Avtorica: Eva Šorn, 8.b Mentor: Boštjan Štih, prof. bio. in kem. Osnovna šola Hudinja Celje, marec
Mestna občina Celje, Mladi za Celje Pridobivanje električne energije z gorivno celico Raziskovalna naloga Avtorica: Eva Šorn, 8.b Mentor: Boštjan Štih, prof. bio. in kem. Osnovna šola Hudinja Celje, marec
JEDILNIK SEPTEMBER 2004
 1.5.2019 PRAZNIK 2.5.2019 3.5.2019 pšenični zdrob na nehomogeniziranem mleku (po želji s čokoladnim posipom) / PRAZNIK goveji golaž koruzna polenta 1 6.5.2019 kakav z nehomogeniziranim mlekom mlečna pletenka
1.5.2019 PRAZNIK 2.5.2019 3.5.2019 pšenični zdrob na nehomogeniziranem mleku (po želji s čokoladnim posipom) / PRAZNIK goveji golaž koruzna polenta 1 6.5.2019 kakav z nehomogeniziranim mlekom mlečna pletenka
PONEDELJEK, TOREK, SREDA, ČETRTEK, PETEK, ZAJTRK GRAHAM KRUH(1,6,11), KREM MASLO(7) BELA ŽITNA
 1. 1. 2018 2. 1. 2018 3. 1. 2018 4. 1. 2018 5. 1. 2018 KRUH(1,6,11), KREM MASLO(7) BELA ŽITNA KAVA(1,6,7) MAKOVA ŠTRUČKA(1,6), POLENTA,, KRUH(1,6,11) MANDARINE JABOLKA ANANAS PRAZNIK PRAZNIK KRUH(1,6,11),
1. 1. 2018 2. 1. 2018 3. 1. 2018 4. 1. 2018 5. 1. 2018 KRUH(1,6,11), KREM MASLO(7) BELA ŽITNA KAVA(1,6,7) MAKOVA ŠTRUČKA(1,6), POLENTA,, KRUH(1,6,11) MANDARINE JABOLKA ANANAS PRAZNIK PRAZNIK KRUH(1,6,11),
Microsoft Word - P-55 EKO PUFER z manj alkohola.doc
 VARNOSTNI LIST Stran 1 od 6 Datum izdaje: 3. 5. 2000 Datum revidirane revizije: 28. 5. 2008 Štev. revidirane revizije: 6 1. Identifikacija snovi / pripravka in podatki o dobavitelju: Identifikacija snovi
VARNOSTNI LIST Stran 1 od 6 Datum izdaje: 3. 5. 2000 Datum revidirane revizije: 28. 5. 2008 Štev. revidirane revizije: 6 1. Identifikacija snovi / pripravka in podatki o dobavitelju: Identifikacija snovi
OD IN MALICA KOSILO PONEDELJEK / ALERGENI TOREK / ALERGENI SREDA POLNOZRNATA BOMBETKA, PIŠČANČJA POSEBNA SALAMA, POLMASTNI SIR, K
 OD 01. 01. IN 05. 01. 2018 PONEDELJEK / ALERGENI / ALERGENI POLNOZRNATA BOMBETKA, PIŠČANČJA POSEBNA SALAMA, POLMASTNI SIR, KISLE KUMARE, PLANINSKI ČAJ Z MEDOM SEGEDIN GOLAŽ, KORUZNA POLENTA, PUDING S SMETANO
OD 01. 01. IN 05. 01. 2018 PONEDELJEK / ALERGENI / ALERGENI POLNOZRNATA BOMBETKA, PIŠČANČJA POSEBNA SALAMA, POLMASTNI SIR, KISLE KUMARE, PLANINSKI ČAJ Z MEDOM SEGEDIN GOLAŽ, KORUZNA POLENTA, PUDING S SMETANO
VARNOSNI LIST
 Ime izdelka Belinka Tophybrid Stran 1 od 5 1. IDENTIFIKACIJA ZMESI IN DRUŽBE/PODJETJA 1.1 Identifikator izdelka: Ime pripravka: Koda: 479842 BELINKA TOPHYBRID 1.2 Pomembne identificirane uporabe zmesi
Ime izdelka Belinka Tophybrid Stran 1 od 5 1. IDENTIFIKACIJA ZMESI IN DRUŽBE/PODJETJA 1.1 Identifikator izdelka: Ime pripravka: Koda: 479842 BELINKA TOPHYBRID 1.2 Pomembne identificirane uporabe zmesi
Ljubljana,11
 DIETNI JEDILNIK ZA OTROKE 1. STAROSTNEGA OBDOBJA - DIETA brez mleka, jajc, soje, arašidov in oreščkov, jagod, sezama (vzg. Andreja, E. Mo) Koruzni kruh (B forma)* Polnozrnata žemlja*, Dietno pecivo*, Jabolko,
DIETNI JEDILNIK ZA OTROKE 1. STAROSTNEGA OBDOBJA - DIETA brez mleka, jajc, soje, arašidov in oreščkov, jagod, sezama (vzg. Andreja, E. Mo) Koruzni kruh (B forma)* Polnozrnata žemlja*, Dietno pecivo*, Jabolko,
Ljubljana,11
 DIETNI JEDILNIK ZA OTROKE 1. STAROSTNEGA OBDOBJA - DIETA brez mleka, jajc, soje, arašidov in oreščkov, jagod, sezama, (vzg. Vida, E. Mo) MOJCA/VJ ZA OBDOBJE OD 29.06. DO 03.07.2015 Bio pšenični kruh* (B-forma),
DIETNI JEDILNIK ZA OTROKE 1. STAROSTNEGA OBDOBJA - DIETA brez mleka, jajc, soje, arašidov in oreščkov, jagod, sezama, (vzg. Vida, E. Mo) MOJCA/VJ ZA OBDOBJE OD 29.06. DO 03.07.2015 Bio pšenični kruh* (B-forma),
OSNOVNA ŠOLA RADA ROBIČA LIMBUŠ
 1. TEDEN od 31. 12. - 4. 1. 19 31. 12. 2019 1. 1. 2019 2. 1. 2019 3. 1. 2019 4. 1. 2019 Koruzni kruh, različni namazi, otroški Čokolešnik, mleko Sirova štručka, z domačim mlekom Mlečni kruh, tamar namaz
1. TEDEN od 31. 12. - 4. 1. 19 31. 12. 2019 1. 1. 2019 2. 1. 2019 3. 1. 2019 4. 1. 2019 Koruzni kruh, različni namazi, otroški Čokolešnik, mleko Sirova štručka, z domačim mlekom Mlečni kruh, tamar namaz
CARAMBA Profi Hochleistungs Synthese-Öl (Aerosol) - CARAMBA Zmogljivo sintetièno olje (aerosole)(SI)
 stran: 1 / 9 * ODDELEK 1: Identifikacija snovi/zmesi in družbe/podjetja 1.1 Identifikator izdelka 1.2 Pomembne identificirane uporabe snovi ali zmesi in odsvetovane uporabe Druge relevantne informacije
stran: 1 / 9 * ODDELEK 1: Identifikacija snovi/zmesi in družbe/podjetja 1.1 Identifikator izdelka 1.2 Pomembne identificirane uporabe snovi ali zmesi in odsvetovane uporabe Druge relevantne informacije
JEDILNIK OD 3.1. DO PONEDELJEK PRAZNIK TOREK PRAZNIK SREDA MALICA: ovseni kruh (1), namaz s čičeriko (7), čaj z medom, jabolko KOSILO: telečj
 JEDILNIK OD 3.1. DO 5.1.2018 PRAZNIK PRAZNIK MALICA: ovseni kruh (1), namaz s čičeriko (7), čaj z medom, jabolko KOSILO: telečja obara (1,3), rižev narastek (3,7), eko sok MALICA 1. star. obd.: rozine
JEDILNIK OD 3.1. DO 5.1.2018 PRAZNIK PRAZNIK MALICA: ovseni kruh (1), namaz s čičeriko (7), čaj z medom, jabolko KOSILO: telečja obara (1,3), rižev narastek (3,7), eko sok MALICA 1. star. obd.: rozine
Microsoft Word - januar2019 VRTEC.doc
 31. 12. 2018 1. 1. 2019 2. 1. 2019 3. 1. 2019 kruh s semeni, kisla smetana, džem, sadni čaj 4. 1. 2019 polnozrnata štručka, trdo kuhana jajčka, rdeča paprika, otroški čaj gobova juha, pečen file osliča,
31. 12. 2018 1. 1. 2019 2. 1. 2019 3. 1. 2019 kruh s semeni, kisla smetana, džem, sadni čaj 4. 1. 2019 polnozrnata štručka, trdo kuhana jajčka, rdeča paprika, otroški čaj gobova juha, pečen file osliča,
DATUM
 31. 12. 2018 DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA sirni namaz (mleko), črni kruh - cvetačna juha, makaronovo meso topljeni sir (mleko), pol bel (gluten, soja,, otroški (gluten, jajce soja,, rdeča
31. 12. 2018 DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA sirni namaz (mleko), črni kruh - cvetačna juha, makaronovo meso topljeni sir (mleko), pol bel (gluten, soja,, otroški (gluten, jajce soja,, rdeča
JEDILNIK ZA MESEC JUNIJ starostno obdobje Ponedeljek, ZAJTRK MALICA KOSILO POP. MALICA I. meni mlečni pšenični zdrob (vsebuje alerg
 JEDILNIK ZA MESEC JUNIJ 2019 1. starostno obdobje 3. 6. 2019 POP. I. meni mlečni pšenični zdrob (vsebuje alergene: laktoza, gluten), II. meni pizza (vsebuje alergene: gluten, soja, sezam), planinski čaj
JEDILNIK ZA MESEC JUNIJ 2019 1. starostno obdobje 3. 6. 2019 POP. I. meni mlečni pšenični zdrob (vsebuje alergene: laktoza, gluten), II. meni pizza (vsebuje alergene: gluten, soja, sezam), planinski čaj
Zavod sv. Stanislava Škofijska klasična gimnazija VPLIV KISLEGA DEŽJA NA RASTLINE poskus pri predmetu biologija
 Zavod sv. Stanislava Škofijska klasična gimnazija VPLIV KISLEGA DEŽJA NA RASTLINE poskus pri predmetu biologija KAZALO: 1 UVOD...3 2 MATERIAL...4 POSTOPEK...4 3 SKICA NASTAVITVE POSKUSA...5 4 REZULTATI...6
Zavod sv. Stanislava Škofijska klasična gimnazija VPLIV KISLEGA DEŽJA NA RASTLINE poskus pri predmetu biologija KAZALO: 1 UVOD...3 2 MATERIAL...4 POSTOPEK...4 3 SKICA NASTAVITVE POSKUSA...5 4 REZULTATI...6
Microsoft Word - M docx
 Državni izpitni center *M1180314* SPOMLADANSKI IZPITNI ROK Izpitna pola Modul gradbeništvo NAVODILA ZA OCENJEVANJE Četrtek, 14. junij 01 SPLOŠNA MATURA RIC 01 M11-803-1-4 IZPITNA POLA Modul gradbeništvo
Državni izpitni center *M1180314* SPOMLADANSKI IZPITNI ROK Izpitna pola Modul gradbeništvo NAVODILA ZA OCENJEVANJE Četrtek, 14. junij 01 SPLOŠNA MATURA RIC 01 M11-803-1-4 IZPITNA POLA Modul gradbeništvo
PowerPoint Presentation
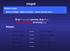 Integral rešujemo nalogo: Dana je funkcija f. Najdimo funkcijo F, katere odvod je enak f. Če je F ()=f() pravimo, da je F() primitivna funkcija za funkcijo f(). Primeri: f ( ) = cos f ( ) = sin f () =
Integral rešujemo nalogo: Dana je funkcija f. Najdimo funkcijo F, katere odvod je enak f. Če je F ()=f() pravimo, da je F() primitivna funkcija za funkcijo f(). Primeri: f ( ) = cos f ( ) = sin f () =
PowerPointova predstavitev
 MOŽNOSTI ZDRAVLJEN DIETA PRI LEDVIČNI BOLEZNI Razumeti ledvično bolezen, njen potek in vedeti za možnosti zdravljenja KAJ DELAJO LEDVICE čistijo kri in odstranjujejo odvečno vodo iz telesa odstranjujejo
MOŽNOSTI ZDRAVLJEN DIETA PRI LEDVIČNI BOLEZNI Razumeti ledvično bolezen, njen potek in vedeti za možnosti zdravljenja KAJ DELAJO LEDVICE čistijo kri in odstranjujejo odvečno vodo iz telesa odstranjujejo
Atomska spektroskopija PROSTI ATOMI VZBUJENI ATOMI Marjan Veber Metode atomske/elementne masne/ spektrometrije Elektronska konfiguracija Mg
 Atomska spektroskopija PROSTI ATOMI VZBUJENI ATOMI Metode atomske/elementne masne/ spektrometrije Elektronska konfiguracija Mg Mg e 1s 2s2p 3d 4s 3p 3s e Po dogovoru ima osnovno elektronsko stanje energijo
Atomska spektroskopija PROSTI ATOMI VZBUJENI ATOMI Metode atomske/elementne masne/ spektrometrije Elektronska konfiguracija Mg Mg e 1s 2s2p 3d 4s 3p 3s e Po dogovoru ima osnovno elektronsko stanje energijo
Takoj ko vstanemo 1 dcl
 1.Dan PREHRANA NA DAN TELOVADBE Zajtrk Gr. Kcal Belj. Oglj. Maš. 2 dcl toplega mleka 1,6% mm 200 90 6,6 9,9 2,8 Muesli z vlakninami (Dorset cereals) 50 186 4 36 3,5 Skupaj 286,8 11,2 46,2 6.9 Malica 1:
1.Dan PREHRANA NA DAN TELOVADBE Zajtrk Gr. Kcal Belj. Oglj. Maš. 2 dcl toplega mleka 1,6% mm 200 90 6,6 9,9 2,8 Muesli z vlakninami (Dorset cereals) 50 186 4 36 3,5 Skupaj 286,8 11,2 46,2 6.9 Malica 1:
Stolpec1 Stolpec2 Stolpec3 JEDILNIK mesec maj Datum Malica Kosilo Popoldanska malica Sreda PRAZNIK PRAZNIK Četrtek PRAZNIK PRAZNIK
 Sreda PRAZNIK PRAZNIK 01.05.2019 Četrtek PRAZNIK PRAZNIK 02.05.2019 Petek POUKA PROST DAN POUKA PROST DAN 03.05.2019 Ponedeljek mleko in sadje (ŠS) cvetačna juha jabolčni krhlji makaronovo meso 06.05.2019
Sreda PRAZNIK PRAZNIK 01.05.2019 Četrtek PRAZNIK PRAZNIK 02.05.2019 Petek POUKA PROST DAN POUKA PROST DAN 03.05.2019 Ponedeljek mleko in sadje (ŠS) cvetačna juha jabolčni krhlji makaronovo meso 06.05.2019
ENOTA 1 Izvor hrane Klasifikacija in funkcija hrane Kako se bomo učili? Page Izvor hrane. 2 Skupine hrane... 5 Funkcija hrane 7 KAJ SE BOMO NAUČILI? -
 ENOTA 1 Izvor hrane Klasifikacija in funkcija hrane Kako se bomo učili? Page Izvor hrane. 2 Skupine hrane... 5 Funkcija hrane 7 KAJ SE BOMO NAUČILI? - Kakšnega izvora je hrana ki jo jemo: živalskega, rastlinskega
ENOTA 1 Izvor hrane Klasifikacija in funkcija hrane Kako se bomo učili? Page Izvor hrane. 2 Skupine hrane... 5 Funkcija hrane 7 KAJ SE BOMO NAUČILI? - Kakšnega izvora je hrana ki jo jemo: živalskega, rastlinskega
1
 Stran 1 od 5 1. IDENTIFIKACIJA SNOVI ALI PRIPRAVKA IN PODATKI O DOBAVITELJU Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka: Dodatek za injekcijsko maso. INJEKTIN F3 Proizvajalec: TKK Proizvodnja
Stran 1 od 5 1. IDENTIFIKACIJA SNOVI ALI PRIPRAVKA IN PODATKI O DOBAVITELJU Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka: Dodatek za injekcijsko maso. INJEKTIN F3 Proizvajalec: TKK Proizvodnja
Microsoft Word - Softshell Proof _Wash-In_ 45 SDS SLV V2.doc
 Varnostni List SOFTSHELL PROOF (Wash-In) ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: SOFTSHELL PROOF (Wash-In) Koda izdelka: 45 1.2. Pomembne identificirane uporabe
Varnostni List SOFTSHELL PROOF (Wash-In) ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: SOFTSHELL PROOF (Wash-In) Koda izdelka: 45 1.2. Pomembne identificirane uporabe
DATUM
 3. 6. DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA Jagode čokolešnik s toplim mlekom kakav (mleko, oreščki), topljeni kostna juha z rezanci (gluten, jabolčni žepek (gluten, soja, (gluten, soja, mleko,
3. 6. DATUM ZAJTRK MALICA KOSILO POPOLDANSKA MALICA Jagode čokolešnik s toplim mlekom kakav (mleko, oreščki), topljeni kostna juha z rezanci (gluten, jabolčni žepek (gluten, soja, (gluten, soja, mleko,
