Uvod v OGRRANSKO KEMIJO / KEMIJO OGLKIKOVODIKOV in njihovih DERIVATOV Elementna sestava: SNOVI in SPOJINE Anorganske snovi vsi elementi (razen žlahtni
|
|
|
- Jolanda Mihelič
- pred 4 leti
- Pregledov:
Transkripcija
1 Uvod v OGRRANSKO KEMIJO / KEMIJO OGLKIKOVODIKOV in njihovih DERIVATOV Elementna sestava: SNOVI in SPOJINE Anorganske snovi vsi elementi (razen žlahtnih plinov) Organske snovi C(ogljik),H(vodik),O(kisik), N(dušik), S(žveplo), [Pvčasih fosfor], halogeni elementi Vezi: jonske vezi -pogostejše kovalentne Lastnosti: - topnost v H 2 O: boljše topne slabše topne - gorljivost: slabše/težje gorljive boljše/lažje gorljive - obstojnost s.: na segrevanje obstojnejše na segrevanje manj obstojne Število spojin: približno ½ milijona več kot 2 milijonov
2 DOKAZI ELEMENTOV v organskih snoveh: Vse organske snovi vsebujejo ogljik(c), vodik(h), kisik(o), dušik(n), žveplo(s), včasih fosfor(p), halogeni elementi (fluor-f, klor-cl, brom-br, jod- I). Dokaz ogljika: Z OKSIDACIJO POOGLENITEV: o snov segrevamo o če poogleni dokaz za OGLJIK & da je snov ORGANSKA o (npr.: segrevanje sladkorjakaramelapoogleni) DODAJANJE BAKROVEGA OKSIDA [CuO]: o snov segrevamo o ogljik se spoji/oksidira s kisikom nastane CO 2, ki ga uvajamo v epruveto o CO 2 dokažemo s apneno vodo/apnico[ca(oh) 2 ] postane motno-bela oborina: Ca(OH) 2 + CO 2 CaCO 3 (motno) + H 2 O 2. Dokaz za vodik: Z OKSIDACIJO o snovi dodamo bakrov oksid [CuO] o vodik v snovi oksidira v H 2 O, ki ga dokažemo s CuSO 4 (bel) o CuSO 4 damo na steno epruvete, če pride v stik z nastalo vodo nastane modra galica[cuso 4 5H 2 O]: CuSO 4 +5H 2 O CuSO 4 5H 2 O 3. Dokaz za kisik: NE DOKAZUJEMO Dušik, žveplo in halogene elemente preden jih dokazujemo pretvorimo v ione. To naredimo z RAZKLOPOM = pretvorba kovalentnih vezi v ionske vezi.. vzorcu v epruveti dodamo REDUCENT: Na ali Mg/Na 2 CO 3 2. segrevamo, tako da steklo "rdeče" zažari 3. na hitro ohladimo v mrzli vodi 4. epruveta poči 5. v vodi so tako koščki stekla med novonastalimi ioni 6. filtriramo (v filtratu-(čaši) proučujemo ione) 4. Dokaz za dušik: Z REDUKCIJO o naredimo razklop o v filtratu lahko imamo več različnih dušikovih ionov: - NH 4+ (amonijevi ioni): - CN - (cianidni ioni) 2
3 - SCN - (tiocianatni/rodanidni ioni) Dokaz za NH 4+ : o raztopina je zelo bazična (saj smo na začetku pri razklopu dodali Mg in Na ki z vodo reagira bazično) o dokažemo ga z rdečim lakmusovim papirjem, ki se zaradi izhajanja amonijevega plina obarva modro Dokaz za CN - : o dodamo Fe 3+ ali Fe 2+ in pri ustreznem ph o CN - + Fe 3+ /Fe 2+ /Ph Fe 4 [Fe(CN) 6 ] 3 berlinsko modrilo Dokaz za SCN - : o SCN - + Fe 3+ obarva se krvavo rdeče 5. Dokaz za žveplo: Z REDUKCIJO če je skupaj z N nastane SCN dokaz za samo žveplo: o dodamo svinčeve ione + ocetno kislino o nastane črna oborina dokaz za sulfidne ione o S 2- + Pb 2+ + ocetna kislina PbS 6. Dokaz za halogenide: Z REDUKCIJO če so skupaj z sulfidnimi ioni: o moramo te odstraniti-s kislino H 2 SO 4 koncentrirana žveplova k. (saj bi lahko reagiral z AgNO 3 tako bi nastala črna oborina, ki bi prekrila dokaze za vse druge halogenide, ki so svetlejše barve) o segrevamo sulfidne ione o ko jih odstranimo jih dokažemo z: S 2- + H 3 O + H 2 S ( izhlapi) o halogenidni ioni: Cl - + AgNO 3 AgCl (bela) Br - + AgNO 3 AgBr (belo-rumena) I - + AgNO 3 AgI (rumena) dokaz za plemensko reakcijo-[dokažemo samo halogene elemente, ne ugotovimo pa točno kateri element nastopa]: o baker segrevamo (oksidira, zaradi prisotnosti kisikapostne črno) o pomočimo v vzorec o ponovno segrevamo vsi halogenidi gorijo z značilnim zelenim plamenom POSKUSI: razklop dušik poskus poteka v degistoriju vzorcu dodamo reducent ( Mg/Na 2 CO 3 ) epruveto z vzorcem segrevamo-3min, da zažari (opazimo vijolično & rumeno sklepamo da je v vzorcu I in S) epruveta čašo v kateri poogleni so koščki (dokaz stekla ogljika) + ioni vzorca pokrijemo z urnim stekelcem + omočenim rdečim lakmusovim papirjem lakmusov papir se obarva modro v čaši z koščki stekla + ioni vzorca (črna oborina) 3
4 S 2- CN - S - SCN - filtriramo, da dobimo bistro tekočino izmerimo ph: je zelo bazičen, saj smo dodali prej natrijev karbonat = ph=0 dodamo svinčeve ione v epruveto, v katero smo prej uvajali ione črno/rjava raztopina S -2 + Pb 2+ PbS v filtrat dodamo ocetno kislino (CH 3 COOH) segrevamo da ugotovimo če je še vedno prisotnih kaj žveplovih ionov v vzorcu (bi se obarvalo črno) dodamo Fe 3+ dokaz za cianidne ione se obarva črno, namesto berlinsko modrilo(pri nas niso prisotni) dodamo kislino se ne obarva črno sulfidni ioni niso prisotni v vzorec damo Fe +3 obarva se krvavo rdeče dokaz da so prisotni tiocianidni ioni elementihalogeni elementarni I imamo filtrat brez sulfidnih ionov dodamo AgNO 3 obarva se rumeno: dokaz za I plemenska reakcija: segrevamo baker pomočimo v vzorec segrevamo dobimo zelen plamen dokaz za halogenidne ione jodove ione pretvorimo v elementarni I: dodamo močnejši oksidant (HNO 3 -koncentrirana, kot oksidant) dobimo temno rumeno barvo dodamo kloroform (CHCl 3 ) postane roza/vijolično dokaz za elementarni I 4
5 VEZI Vezi znotraj molekul: kovalentne ionske kovinske Vodikove vezi Vezi med molekulami: disperzijske indukcijske orientacijske. VEZI ZNOTRAJ MOLEKULE: (močne: nekaj 00 Kj/mol) Kovalentne vezi: Nastanek: samska elektrona se povežeta in združita s prekrivanjem orbital Polarnost: Nepolarnost: A : B oba atoma sta enako močna, zato oba privlačita vezni par z enako močjo Polarnost: A :B to je kovalentna polarna vez, ker en element bolj privlači vezni par kot drug, ker je bolj elektronegativen ELEKTRONEGATIVNOST: je sposobnost atoma, da privlači vezne elektrone (po periodi: narašča, po skupini: pada) POL: δ + δ - na negativnem polu je večja elektronska gostota na pozitivnem polu je manjša elektronska gostota manjša elektronska gostota večja elektronska gostota Ionske vezi: en atom drugemu odtrga elektron in tako postane negativni ion, ANION, drug pa je pozitivni KATION večja kot je razlika pri elektronegativnosti, bolj je vez polarna POLARNOST MOLEKULE: je odvisna od ne-simetričnosti molekule Primer: CCl 4 ogljikov tetraklorid vezi: kovalentne, polarne molekula: nepolarna ker je simetrična, naboj je enakomerno porazdeljen Kovinske vezi: jih ni v organski kemiji 2. VODIKOVA VEZ: (20 kj/mol) pojavi se, ko se H veže na najbolj elekrtonegativne elemente 5
6 kisik skupni elektronski par preveč privlači vodik čuti primanjkljaj vodik se tako poveže z drugim mestom, ki je zelo elekrtonegativen (voda tako tvori 4 vezi z okolico) pomembna je zaradi: vpliva na vrelišče (je višje) vpliva na gostoto izparilno toploto topnost v vodi 3. VEZI MED MOLEKULAMI: (00x šibkejše, kot vezi znotraj molekul) od njih se odvisne fizikalne lastnosti: vrelišče tališče agregatno stanje (topnost) Disperzijske vezi: edine vezi med nepolarnimi molekulami so povsod prisotne moč je odvisna od velikosti molekule (večje kot so molekule, močnejše so disperzijske vezi molekule so močneje povezane) zaradi naključnega gibanja elektronov se v molekuli v vsakem trenutku izpostavljajo poli Orientacijske vezi: samo med polarnimi molekulami bolj kot so molekule polarne, močnejše so vezi med polarnimi molekulami, ki imajo pole deluje privlak ORIENTACIJSKA VEZ (+ in -), gibljejo se tako, da se z nasprotnimi poli gibljejo druga proti drugi DIPOL DIPOL INTERAKCIJA: medsebojni vpliv dveh polov med dvema sosednjima polarnima molekulama 6
7 Narava OGLJIKOVEGA ATOMA: Ogljik lahko tvori zelo veliko različnih spojin, ker: se lahko povezuje v verige, ki so različno dolge verige so lahko različno razvejane lahko se veže v obroče povezuje se z različnimi vezmi (enojnimi, dvojnimi, trojnimi, ) možnih je veliko načinov povezovanja zato poznamo veliko vrst organskih spojin NAČINI POVEZOVANJA:. Nastanek enojne vezi: sp 3 v organskih spojinah tvori 4 vezi: elektronska konfiguracija: 6C s 2 2s 2 2p x 2p y vzburjeno stanje s 2 2s 2p x 2p y 2p z [tvori 4 vezi] HIBRIDIZACIJA: računski postopek,ki atomske orbitale pretvori v enako št. tako imenovanih hibridnih orbital. Te so med seboj enake po obliki, energiji, v prostoru pa skušajo biti usmerjene tako, da so čim bolj narazen druga od druge metan o ima nižjo energijo kot 2p x o pri metanu so koti med vezmi 09 28' o Vrsta hibridizacije: sp 3 o pretvorimo: s 2 2s 2 2p x 2p y 2p z s 2 2(sp 3 ) 2(sp 3 ) 2(sp 3 ) 2(sp 3 ) o so enako močne o v obliki tetraedra o povprečje energij o nastane enojna vez: prekrijeta se z enojnim/čelnim prekrivanjem nastane sigma vez (močna vez) 7
8 moč: E = 346 kj mol - dolžina vezi:d =, m (dolžina med jedroma sosednjih molekul) 2. Nastanek dvojen vezi: sp 2 6 C s 2 2s 2 2p x 2p y v.s. s 2 2s 2p x 2p y 2p z 2p orbitali] s 2 2(sp 2 ) 2(sp 2 ) 2(sp 2 ) 2p z [pretvorimo s in o koti: v isti ravnini: 20 o vezi: sigma vez vez) pi-vezi(pravokotno prebadata sigma o moč: E = 60 kj mol - (saj imamo eno sigma-močno vez in eno pišibko vez) o dolžina vezi: d =, m 3. Nastanek trojne vezi: sp ležijo na isti premici 6 C s 2 2s 2 2p x 2p y v.s. s 2 2s 2p x 2p y 2p z hibridizacija sp s 2 (2sp) (2sp) 2p y 2p z so pravokotne med sabo sigma vez + 2 pi vezi o moč: E = 80 kj mol - (vse vezi se povežejo v oblak, zato so močne) o dolžina: d =, m (ker je več v3ezi, je molekula močnejša, potegne vezi bolj k sebi zato je vez krajša) 4. Nastanek vezi v ARENIH: sp 2 predstavnik: benzen pravilni 6-kotnik d=, m (vezi so enako dolge) vezi: med enojnimi in dvojnimi vezmi molekula je polarna ker leži v ravnini 8
9 HIPRIDIZACIJA: sp 2 (v ravnini) 6C s 2 2s 2 2p x 2p y v.s. s 2 2s 2p x 2p y 2p z 2p orbitali] s 2 (2sp 2 ) (2sp 2 ) (2sp 2 ) 2p z [pretvorimo s in DELOKALIZIRANA π VEZ: razprostrta pi vez (lastnosti ima med enojno in dvojno vezjo) 9
10 . EMPIRIČNA FORMULA: NaCl: razmerje je : CH 2 : razmerje je :2 Formule Organskih spojin: 2. MOLEKULSKA FORMULA: H 2 SO 4 : dva H, en S, štirje O C 6 H 2 : šest C-atomov in dvanajst H-atomov 3. STRUKTURNA FROMULA: 4. RACIONALNA FORMULA: CH 3 CH 2 CH 2 CH 2 CH 2 CH 3 (poznamo strukturo) 5. SKELETNA FORMULA: uporabljamo za velike, dolge formule benzen tako označujemo tudi dvojne, trojne vezi vodika označimo vse elemente, razen ogljika in 6. PROSTORSKA ali STEREOKEMIJSKA FORMULA: (pove nam kako atomi ležijo v prostoru) je v ravnini "štrli" naprej "štrli" nazaj 0
11 NOMENKLATURA Organskih Spojin (IUPAC nomenklatura) PREDPONA KOREN KONČNICA Poimenovanje OGLJIKOVODIKOV: Z ravno verigo: same enojne vezi: ALKANI o C-atom: metan o o 2 C-atom: etan o o 3 C-atom: propan o o 4 C-atom: butan o o 5 C-atom: pentan o 6 C-atom: heksan 7 C-atom: heptan 8 C-atom: oktan 9 C-atom: nonan 0 C-atom: dekan same dvojne vezi: ALKENI o CH 3 CH 2 CH = CH 2 but en o CH 2 = CH - CH 2 CH = CH 2 penta,4 di en o (di- dve dvojne vezi, tri-tri trojne vezi) o (štejemo tako, da so vezi najbližje) - : mono - 6: heksa - 2: di - 7: hepta - 3: tri - 8: okta - 4: tetra - 9: nona - 5: penta - 0: deka same trojne vezi: ALKINI o CH C CH 3 PROPIN [GRŠKA ŠTEVILKA + IN] Z razvejano verigo: same enojne vezi: o poiščemo ravno vez(tako da je najdaljša) & preštejemo C- atome-določimo ime (oktan) o označimo & preštejemo druge vezi (3-dimetil, 5-etil) o stranske veje napišemo po abecedi, glede na grške predpone (5-etil, 3-dimetil) 5-etil-3, 3-dimetil oktan 2,4 - dimetilheptan Z obroči:
12 o predpona ciklo cikloheksan o če imamo dvojno vez: začnemo šteti pri eni dvojni vezi, naprej pa v taki smeri, da bo druga vez čim bližje cikloheksa-,4- dien o če je benzen stranska veja benezen poimenujemo FENIL feniletan o (benzen, kot glavna veja) etilbenzen 2 Poimenovanje spojin z FUNKCIONALNIMI SKUPINAMI: Ene funkcionalne skupine so samo v predponi Večina funkcionalnim skupin je v končnici in predponi: če je v molekuli ena vrsta funkcionalne skupine, pride ta v končnico 2
13 če je v molekuli več različnih funkcionalnih skupin, pride v končnico tista, ki prevladuje, ostale pa v predpono funkcionalna skupina predpona končnica NO 2 nitro- F fluoro- Cl kloro- Br bromo- I jodo- OH hidroksi- -ol (formil-) -al (okso-) -on COOH -ojska kislina NH 2 amino- -amin CN ciano- - nitril 3
14 IZOMERIJA o IZOMERIJA: je pojav, da imajo snovi enake molekulske formule, a različno zgradbo, in s tem tudi različne lastnosti o med sabo sorodne spojine so IZOMERI o VRRIŽNA IZOMERIJA: veriga je različno razvejana o PRIMARNI C-ATOM: C-atom, ki se na sosednje C-atome veže z samo eno enojno vezjo o SEKUNDARNI: o TERCIARNI: o KVARTARNI: o MULTIPNA VEZ: skupen izraz za dvojno ali trojno vez o VRSTE IZOMERIJ: Strukturna izomerija: Stereoizomerija: je pojav, kjer imajo snovi enako molekulsko formulo a različno strukturno formulo snovi imajo enako molekulsko in strukturno formulo, razlikujejo pa se po legi atomov v prostoru - skeletna izomerija - položajna izomerija - funkcionalna izomerija - geometrijska izomerija - optična izomerija. STRUKTURNA IZOMERIJA: o Skeletna izomerija: pojav, kjer imajo snovi enako molekulsko formulo, a različno skeletno formulo 4
15 o Položajna izomerija: pojav, kjer imajo snovi enako molekulsko formulo, razlikujejo pa se po položaju funkcionalne skupine ali pa po položaju multipne vezi o Funkcionalna izomerija: pojav, kjer imajo snovi enako molekulsko formulo, a različne funkcionalne skupine 2. STEREOIZOMERIJA: o Geometrijska izomerija: je izomerija, možni pri snoveh, v katerih ni vrtljivost okrog vezi med dvema ogljikoma (torej samo pri enojnih vezeh- C=C:se ne more vrteti) CIS OBLIKA: TRANS OBLIKA: spojini v cis in trans obliki sta različni spojini (cis je bolj polarna) o Optična izomerija: je izomerija pri asimetričnih molekulah, ki vsebujejo kiralne centre KIRALNOST: pojav, da sta dve stvar(molekuli) zrcalni sliki druga druge(npr.:roki) KIERALNI CENTER: je ogljikov atom, ki ima nase vezane 4 različne atome(cl, ) ali atomske skupine (OH, ) 5
16 OPTIČNI IZOMERI: imajo enake kemijske in fizikalne lastnosti, razlikujejo pa se po optičnih lastnostih in fiziološkem učinku če v molekulo spustimo vir svetlobe se ta nagne pod določenim kotom njena zrcalna slika pa zasuče svetlobo pod istim kotom, le na drugo stran kako spojina vpliva na telo (dglukoza-njena zrcalna slika je l- glukoza, ki pa je telo ne prepozna kot glukozo, ampak jo obravnava kot balast) RACEMAT: je zmes obeh optičnih izomerov v razmerji : (vedno ga dobimo v laboratoriju) MEZO SPOJINA: vsebuje paeno število kiralnih centrov, ki so med sabo vzporedni 2 n : število možnih izomerov (n število kiralnih centrov) Označevanje optičnih izomerov: - SUČNOST: ko spustimo svetlobo skozi molekulo: če se zasuče v desno jo označimo s + če se zasuče v levo z - RELATIVNA KONFIGURACIJA: primerjamo spojinino razporeditev atomov glede na glicerolaldehid: - ABSOLUTNA KONFIGURACIJA: uporabljamo R in S (ugotovimo za vsako molekulo posebej) 6
IZBIRNI PREDMET KEMIJA 2. TEST B Ime in priimek: Število točk: /40,5t Ocena: 1.) 22,4 L kisika, merjenega pri 0 o C in 101,3 kpa: (1t) A im
 IZBIRNI PREDMET KEMIJA 2. TEST B Ime in priimek: 8. 1. 2008 Število točk: /40,5t Ocena: 1.) 22,4 L kisika, merjenega pri 0 o C in 101,3 kpa: (1t) A ima maso 16,0 g; B ima maso 32,0 g; C vsebuje 2,00 mol
IZBIRNI PREDMET KEMIJA 2. TEST B Ime in priimek: 8. 1. 2008 Število točk: /40,5t Ocena: 1.) 22,4 L kisika, merjenega pri 0 o C in 101,3 kpa: (1t) A ima maso 16,0 g; B ima maso 32,0 g; C vsebuje 2,00 mol
AMIN I
 AMI I Kaj so Amini Amini so zelo razširjene spojine v naravnih ali umetnih organskih snoveh.kemijsko so vezani v barvilih, zdravilih,alkaloidih in polimerih.prosti amini se redko pojavljajo v naravi, nastanejo
AMI I Kaj so Amini Amini so zelo razširjene spojine v naravnih ali umetnih organskih snoveh.kemijsko so vezani v barvilih, zdravilih,alkaloidih in polimerih.prosti amini se redko pojavljajo v naravi, nastanejo
Odgovori na vprašanja za anorgansko kemijo
 Odgovori na vprašanja za anorgansko kemijo 1. Zakon o stalnih masnih razmerjih Masno razmerje reagentov, v katerem se reagenti spajajo, je neodvisno od načina reakcije ter vedno isto. 2. Zakon o mnogokratnih
Odgovori na vprašanja za anorgansko kemijo 1. Zakon o stalnih masnih razmerjih Masno razmerje reagentov, v katerem se reagenti spajajo, je neodvisno od načina reakcije ter vedno isto. 2. Zakon o mnogokratnih
HALOGENI ELEMENTI
 HALOGENI ELEMENTI Halogeni elementi so elementi 7. skupine periodnega sistema elementov (ali VII. skupine). To so fluor, klor, brom in jod. Halogeni spadajo med nekovine. V elementarnem stanju obstajajo
HALOGENI ELEMENTI Halogeni elementi so elementi 7. skupine periodnega sistema elementov (ali VII. skupine). To so fluor, klor, brom in jod. Halogeni spadajo med nekovine. V elementarnem stanju obstajajo
Microsoft Word - M doc
 Š i f r a k a n d i d a t a : ržavni izpitni center *M12143111* SPOMLNSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 7. junij 2012 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Š i f r a k a n d i d a t a : ržavni izpitni center *M12143111* SPOMLNSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 7. junij 2012 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Microsoft Word doc
 [ifra kandidata: Dr `av ni iz pitni center *M* PREDPREZKUS KEMJA zpitna pola Marec / minut Dovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik B
[ifra kandidata: Dr `av ni iz pitni center *M* PREDPREZKUS KEMJA zpitna pola Marec / minut Dovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik B
10. Vaja: Kemijsko ravnotežje I a) Osnove: Poznamo enosmerne in ravnotežne kemijske reakcije. Za slednje lahko pišemo določeno konstanto kemijskega ra
 10. Vaja: Kemijsko ravnotežje I a) Osnove: Poznamo enosmerne in ravnotežne kemijske reakcije. Za slednje lahko pišemo določeno konstanto kemijskega ravnotežja (K C ), ki nam podaja konstantno razmerje
10. Vaja: Kemijsko ravnotežje I a) Osnove: Poznamo enosmerne in ravnotežne kemijske reakcije. Za slednje lahko pišemo določeno konstanto kemijskega ravnotežja (K C ), ki nam podaja konstantno razmerje
Microsoft Word - M docx
 Š i f r a k a n d i d a t a : ržavni izpitni center *M18243121* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Sreda, 29. avgust 2018 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Š i f r a k a n d i d a t a : ržavni izpitni center *M18243121* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Sreda, 29. avgust 2018 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Kako potekajo reakcije oksidacije in redukcije z manganati (VII) v nevtralni do zmerno alkalni raztopini
 VPRAŠANJA ZA ANALIZNO KEMIJO 1.) Kako potekajo reakcije oksidacije in redukcije z manganati(vii) v nevtralni do zmerno alkalni raztopini? Izberite si ustrezen reducent in napišite reakcijo! 2.) Kako reagirajo
VPRAŠANJA ZA ANALIZNO KEMIJO 1.) Kako potekajo reakcije oksidacije in redukcije z manganati(vii) v nevtralni do zmerno alkalni raztopini? Izberite si ustrezen reducent in napišite reakcijo! 2.) Kako reagirajo
Microsoft Word doc
 [ifra kandidata: r`avni izpitni center *M* PREPREZKUS KEMJ zpitna pola Marec / minut ovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik H ali plasti~no
[ifra kandidata: r`avni izpitni center *M* PREPREZKUS KEMJ zpitna pola Marec / minut ovoljeno dodatno gradivo in pripomo~ki: kandidat prinese s seboj nalivno pero ali kemi~ni svin~nik svin~nik H ali plasti~no
ELEKTROKEMIJA 1. Izračunajte potencial inertne elektrode v raztopine, ki jo dobimo, če zmešamo 5,0 ml 0,1 M Ce 4+ in 5,0 ml 0,3 M raztopine Fe 2+! (E
 ELEKTROKEMIJA 1. Izračunajte potencial inertne elektrode v raztopine, ki jo dobimo, če zmešamo 5,0 ml 0,1 M Ce 4+ in 5,0 ml 0,3 M raztopine Fe 2+! (E o Fe 2+ /Fe 3+ = 0,771 V) Rez.: 0,735 V 2. Izračunajte
ELEKTROKEMIJA 1. Izračunajte potencial inertne elektrode v raztopine, ki jo dobimo, če zmešamo 5,0 ml 0,1 M Ce 4+ in 5,0 ml 0,3 M raztopine Fe 2+! (E o Fe 2+ /Fe 3+ = 0,771 V) Rez.: 0,735 V 2. Izračunajte
Vsebina Energija pri gorenju notranja energija, entalpija, termokemijski račun, specifična toplota zgorevanja specifična požarna obremenitev
 Vsebina Energija pri gorenju notranja energija, entalpija, termokemijski račun, specifična toplota zgorevanja specifična požarna obremenitev P i entropija, prosta entalpija spontani procesi, gorenje pri
Vsebina Energija pri gorenju notranja energija, entalpija, termokemijski račun, specifična toplota zgorevanja specifična požarna obremenitev P i entropija, prosta entalpija spontani procesi, gorenje pri
PERIODNI SISTEM 1. skupina
 PERIODNI SISTEM 1. skupina OSNOVNA DEJSTVA & POJMI Vsi elementi so zelo reaktivni, zato jih hranimo pod pertolejem in vsi so mehke, srebrno bele kovine Vse spojine so ionske in topne Vsi elementi, oz.
PERIODNI SISTEM 1. skupina OSNOVNA DEJSTVA & POJMI Vsi elementi so zelo reaktivni, zato jih hranimo pod pertolejem in vsi so mehke, srebrno bele kovine Vse spojine so ionske in topne Vsi elementi, oz.
DELOVANJE KATALIZATORJEV Cilji eksperimenta: Opazovanje delovanja encima katalaze, ki pospešuje razkroj vodikovega peroksida, primerjava njenega delov
 DELOVANJE KATALIZATORJEV Cilji eksperimenta: Opazovanje delovanja encima katalaze, ki pospešuje razkroj vodikovega peroksida, primerjava njenega delovanja z delovanjem nebeljakovinskih katalizatorjev in
DELOVANJE KATALIZATORJEV Cilji eksperimenta: Opazovanje delovanja encima katalaze, ki pospešuje razkroj vodikovega peroksida, primerjava njenega delovanja z delovanjem nebeljakovinskih katalizatorjev in
Microsoft PowerPoint vaja-salen
 Sinteza mimetika encima SD 1. stopnja: H 2 salen 18/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza N,N - bis(saliciliden)etilendiamina Predlagajte orositveni reagent za detekcijo poteka reakcije in za
Sinteza mimetika encima SD 1. stopnja: H 2 salen 18/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza N,N - bis(saliciliden)etilendiamina Predlagajte orositveni reagent za detekcijo poteka reakcije in za
ALKOHOLI
 ALKOHOLI Kaj je alkohol? Alkohol je bistvena učinkovina v alkoholnih pijačah, ter alkoholi so pomembna skupina organskih spojin. V kemiji je alkohol splošen pojem, ki ga uporabljamo za vsako organsko spojino,
ALKOHOLI Kaj je alkohol? Alkohol je bistvena učinkovina v alkoholnih pijačah, ter alkoholi so pomembna skupina organskih spojin. V kemiji je alkohol splošen pojem, ki ga uporabljamo za vsako organsko spojino,
KOVINE
 KOVINE Miha Batič Jernej Štublar 1.b, 1 Gimnazija Bežigrad Kazalo Št. Opis Stran 1 Kovine 3 1.1 Kovinska zgradba 2 Metalurgija 5 2.1 Koncentriranje kovinske rude 5 2.2 Kemijska koncentracija 5 2.3 Redukcija
KOVINE Miha Batič Jernej Štublar 1.b, 1 Gimnazija Bežigrad Kazalo Št. Opis Stran 1 Kovine 3 1.1 Kovinska zgradba 2 Metalurgija 5 2.1 Koncentriranje kovinske rude 5 2.2 Kemijska koncentracija 5 2.3 Redukcija
1
 1. Pojme na desni poveži z ustreznimi spojinami in ioni na levi strani glede na njihove lastnosti in uporabo pri vaji določevanja glukoze in saharoze v skupnem vzorcu! Ni nujno, da si vsi pojmi povezani!
1. Pojme na desni poveži z ustreznimi spojinami in ioni na levi strani glede na njihove lastnosti in uporabo pri vaji določevanja glukoze in saharoze v skupnem vzorcu! Ni nujno, da si vsi pojmi povezani!
UVOD ČISTE SNOVI SNOV ločevanje mešanje ZMESI ELEMENT SPOJINE molekule (NaCl, ATOMI (He) MOLEKULE (F 2, Cl 2, Br 2, I 2, H 2, N 2, O 2, P 4, S 8 samo
 UVOD ČISTE SNOVI SNOV ločevanje mešanje ZMESI ELEMENT SPOJINE molekule (NaCl, ATOMI (He) MOLEKULE (F 2, Cl 2, Br 2, I 2, H 2, N 2, O 2, P 4, S 8 samo sobni pogoji!) AGREGATNA STANJA HOMOGENE zmes na pogled
UVOD ČISTE SNOVI SNOV ločevanje mešanje ZMESI ELEMENT SPOJINE molekule (NaCl, ATOMI (He) MOLEKULE (F 2, Cl 2, Br 2, I 2, H 2, N 2, O 2, P 4, S 8 samo sobni pogoji!) AGREGATNA STANJA HOMOGENE zmes na pogled
SANTE/10070/2016-EN ANNEX
 EVROPSKA KOMISIJA Bruselj, 3.3.2017 C(2017) 1372 final ANNEX 1 PRILOGA k UREDBI KOMISIJE (EU) / o spremembi Priloge I k Uredbi (ES) št. 1334/2008 Evropskega parlamenta in Sveta glede uporabe nekaterih
EVROPSKA KOMISIJA Bruselj, 3.3.2017 C(2017) 1372 final ANNEX 1 PRILOGA k UREDBI KOMISIJE (EU) / o spremembi Priloge I k Uredbi (ES) št. 1334/2008 Evropskega parlamenta in Sveta glede uporabe nekaterih
FIZIKALNA STANJA IN UREJENOST POLIMERNIH VERIG Polimeri se od nizkomolekularnih spojin razlikujejo po naravi fizikalnega stanja in po morfologiji. Gle
 FIZIKALNA STANJA IN UREJENOST POLIMERNIH VERIG Polimeri se od nizkomolekularnih spojin razlikujejo po naravi fizikalnega stanja in po morfologiji. Glede na obliko in način urejanja polimernih verig v trdnem
FIZIKALNA STANJA IN UREJENOST POLIMERNIH VERIG Polimeri se od nizkomolekularnih spojin razlikujejo po naravi fizikalnega stanja in po morfologiji. Glede na obliko in način urejanja polimernih verig v trdnem
PROFILES učno gradivo, navodila za učitelje
 Se bom raztopil, če bo deževalo? Slika 1:diamanti (Vir: http://www.idb.it/; 18.10.2015) Slika 2: kristali kuhinjske soli (Vir: https://hr.wikipedia.org/wiki/kuhinjska _sol; 18.10.2015) Modul za poučevanje
Se bom raztopil, če bo deževalo? Slika 1:diamanti (Vir: http://www.idb.it/; 18.10.2015) Slika 2: kristali kuhinjske soli (Vir: https://hr.wikipedia.org/wiki/kuhinjska _sol; 18.10.2015) Modul za poučevanje
Analizna kemija I
 Analizna kemija I 2. Kemija raztopin Kaj je raztopina? Raztopina je zmes ionov ali molekul topljenca v topilu: Prave raztopine so homogene, raztopljeni (dispergirani) delci pa zelo majhni (ioni, molekule);
Analizna kemija I 2. Kemija raztopin Kaj je raztopina? Raztopina je zmes ionov ali molekul topljenca v topilu: Prave raztopine so homogene, raztopljeni (dispergirani) delci pa zelo majhni (ioni, molekule);
Microsoft Word - N doc
 Š i f r a u ~ e n c a: r`avni izpitni center *N072433* NKNNI ROK KEMIJ PREIZKUS ZNNJ Petek,. junija 2007 / 60 minut ovoljeno gradivo in pripomo~ki: u~enec prinese s seboj modro/~rno nalivno pero ali moder/~rn
Š i f r a u ~ e n c a: r`avni izpitni center *N072433* NKNNI ROK KEMIJ PREIZKUS ZNNJ Petek,. junija 2007 / 60 minut ovoljeno gradivo in pripomo~ki: u~enec prinese s seboj modro/~rno nalivno pero ali moder/~rn
GRADIVO ZA POSVETE
 MINISTRSTVO ZA OBRAMBO Uprava Republike Slovenije za zaščito in reševanje in GASILSKA ZVEZA SLOVENIJE MESEC VARSTVA PRED POŽAROM - GRADIVA - Ljubljana, september 2006 Opomba: Gradivo ni lektorirano in
MINISTRSTVO ZA OBRAMBO Uprava Republike Slovenije za zaščito in reševanje in GASILSKA ZVEZA SLOVENIJE MESEC VARSTVA PRED POŽAROM - GRADIVA - Ljubljana, september 2006 Opomba: Gradivo ni lektorirano in
1. Prehajanje snovi skozi celično membrano biološke membrane so izbirno prepustne (uravnavajo svojo kemijsko sestavo) membrana je o meja med celico oz
 1. Prehajanje snovi skozi celično membrano biološke membrane so izbirno prepustne (uravnavajo svojo kemijsko sestavo) membrana je o meja med celico oz. organeli in okoljem o regulator vstopa in izstopa
1. Prehajanje snovi skozi celično membrano biološke membrane so izbirno prepustne (uravnavajo svojo kemijsko sestavo) membrana je o meja med celico oz. organeli in okoljem o regulator vstopa in izstopa
UREDBA KOMISIJE (EU) 2017/ z dne 3. marca o spremembi Priloge I k Uredbi (ES) št. 1334/ Evropskega parlamenta in
 L 58/14 SL UREDBA KOMISIJE (EU) 2017/378 z dne 3. marca 2017 o spremembi Priloge I k Uredbi (ES) št. 1334/2008 Evropskega parlamenta in Sveta glede uporabe nekaterih aromatičnih snovi (Besedilo velja za
L 58/14 SL UREDBA KOMISIJE (EU) 2017/378 z dne 3. marca 2017 o spremembi Priloge I k Uredbi (ES) št. 1334/2008 Evropskega parlamenta in Sveta glede uporabe nekaterih aromatičnih snovi (Besedilo velja za
Atomska spektroskopija PROSTI ATOMI VZBUJENI ATOMI Marjan Veber Metode atomske/elementne masne/ spektrometrije Elektronska konfiguracija Mg
 Atomska spektroskopija PROSTI ATOMI VZBUJENI ATOMI Metode atomske/elementne masne/ spektrometrije Elektronska konfiguracija Mg Mg e 1s 2s2p 3d 4s 3p 3s e Po dogovoru ima osnovno elektronsko stanje energijo
Atomska spektroskopija PROSTI ATOMI VZBUJENI ATOMI Metode atomske/elementne masne/ spektrometrije Elektronska konfiguracija Mg Mg e 1s 2s2p 3d 4s 3p 3s e Po dogovoru ima osnovno elektronsko stanje energijo
1. izbirni test za MMO 2018 Ljubljana, 16. december Naj bo n naravno število. Na mizi imamo n 2 okraskov n različnih barv in ni nujno, da imam
 1. izbirni test za MMO 018 Ljubljana, 16. december 017 1. Naj bo n naravno število. Na mizi imamo n okraskov n različnih barv in ni nujno, da imamo enako število okraskov vsake barve. Dokaži, da se okraske
1. izbirni test za MMO 018 Ljubljana, 16. december 017 1. Naj bo n naravno število. Na mizi imamo n okraskov n različnih barv in ni nujno, da imamo enako število okraskov vsake barve. Dokaži, da se okraske
Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim na
 Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim načrtom. Urejena je v osem poglavij (Varno eksperimentalno
Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim načrtom. Urejena je v osem poglavij (Varno eksperimentalno
PowerPointova predstavitev
 Obravnava kotov za učence s posebnimi potrebami Reading of angles for pupils with special needs Petra Premrl OŠ Danila Lokarja Ajdovščina OSNOVNA ŠOLA ENAKOVREDNI IZOBRAZBENI STANDARD NIŽJI IZOBRAZBENI
Obravnava kotov za učence s posebnimi potrebami Reading of angles for pupils with special needs Petra Premrl OŠ Danila Lokarja Ajdovščina OSNOVNA ŠOLA ENAKOVREDNI IZOBRAZBENI STANDARD NIŽJI IZOBRAZBENI
Geometrija v nacionalnih preverjanjih znanja
 Geometrija v nacionalnih preverjanjih znanja Aleš Kotnik, OŠ Rada Robiča Limbuš Boštjan Repovž, OŠ Krmelj Struktura NPZ za 6. razred Struktura NPZ za 9. razred Taksonomska stopnja (raven) po Gagneju I
Geometrija v nacionalnih preverjanjih znanja Aleš Kotnik, OŠ Rada Robiča Limbuš Boštjan Repovž, OŠ Krmelj Struktura NPZ za 6. razred Struktura NPZ za 9. razred Taksonomska stopnja (raven) po Gagneju I
Slide 1
 Slide 1 OBDELAVA ODPADNE VODE Slide 2 KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE? KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE?! uravnavanje ph, alkalnosti! odstranjevanje ali dodajanje elementov!
Slide 1 OBDELAVA ODPADNE VODE Slide 2 KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE? KAKO POVRNITI PORUŠENI EKOSITEM V PRVOTNO STANJE?! uravnavanje ph, alkalnosti! odstranjevanje ali dodajanje elementov!
1
 1. Izpit: 23.04.1992 1. Skiciraj strukture skupin NO 2+, NO 2, NO 2-! Pripiši sledeče kote O-N-O in razdalje N- O posamezne strukture: Koti: 115,4 o, 180 o in 134,4 o Razdalje:1,20, 1,15 in 1,24 0 A 2.
1. Izpit: 23.04.1992 1. Skiciraj strukture skupin NO 2+, NO 2, NO 2-! Pripiši sledeče kote O-N-O in razdalje N- O posamezne strukture: Koti: 115,4 o, 180 o in 134,4 o Razdalje:1,20, 1,15 in 1,24 0 A 2.
PowerPoint Presentation
 Tehnološki izzivi proizvodnja biometana in njegovo injiciranje v plinovodno omrežje prof. dr. Iztok Golobič Predstojnik Katedre za toplotno in procesno tehniko Vodja Laboratorija za toplotno tehniko Fakulteta
Tehnološki izzivi proizvodnja biometana in njegovo injiciranje v plinovodno omrežje prof. dr. Iztok Golobič Predstojnik Katedre za toplotno in procesno tehniko Vodja Laboratorija za toplotno tehniko Fakulteta
1 Naloge iz Matematične fizike II /14 1. Enakomerno segreto kocko vržemo v hladnejšo vodo stalne temperature. Kako se spreminja s časom temperat
 1 Naloge iz Matematične fizike II - 2013/14 1. Enakomerno segreto kocko vržemo v hladnejšo vodo stalne temperature. Kako se spreminja s časom temperatura v kocki? Kakšna je časovna odvisnost toplotnega
1 Naloge iz Matematične fizike II - 2013/14 1. Enakomerno segreto kocko vržemo v hladnejšo vodo stalne temperature. Kako se spreminja s časom temperatura v kocki? Kakšna je časovna odvisnost toplotnega
Microsoft PowerPoint - −omen_Baènik
 Strupene kovine v izobraževanju kaj in kako? Andreja Bačnik, ZRSŠ Agnes Šömen Joksić, ZZV Koper Vsebina Opravimo z izrazom težke kovine Razmejimo: elementi kovine strupene kovine Biogeokemijsko kroženje
Strupene kovine v izobraževanju kaj in kako? Andreja Bačnik, ZRSŠ Agnes Šömen Joksić, ZZV Koper Vsebina Opravimo z izrazom težke kovine Razmejimo: elementi kovine strupene kovine Biogeokemijsko kroženje
Microsoft PowerPoint - OVT_4_IzolacijskiMat_v1.pptx
 Osnove visokonapetostne tehnike Izolacijski materiali Boštjan Blažič bostjan.blazic@fe.uni lj.si leon.fe.uni lj.si 01 4768 414 013/14 Izolacijski materiali Delitev: plinasti, tekoči, trdni Plinasti dielektriki
Osnove visokonapetostne tehnike Izolacijski materiali Boštjan Blažič bostjan.blazic@fe.uni lj.si leon.fe.uni lj.si 01 4768 414 013/14 Izolacijski materiali Delitev: plinasti, tekoči, trdni Plinasti dielektriki
PRILOGA I OSNOVNA SESTAVA ZAČETNIH FORMUL ZA DOJENČKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti določene v tej prilogi se nanašajo na končno
 PRILOGA I OSNOVNA SESTAVA ZAČETNIH FORMUL ZA DOJENČKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti določene v tej prilogi se nanašajo na končno pripravljeni obrok, ki se kot tak daje v promet ali
PRILOGA I OSNOVNA SESTAVA ZAČETNIH FORMUL ZA DOJENČKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti določene v tej prilogi se nanašajo na končno pripravljeni obrok, ki se kot tak daje v promet ali
PRILOGA II OSNOVNA SESTAVA NADALJEVALNIH FORMUL ZA DOJENČKE IN MAJHNE OTROKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti, določene v Prilogi, s
 PRILOGA II OSNOVNA SESTAVA NADALJEVALNIH FORMUL ZA DOJENČKE IN MAJHNE OTROKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti, določene v Prilogi, se nanašajo na končno pripravljeni obrok, ki se kot
PRILOGA II OSNOVNA SESTAVA NADALJEVALNIH FORMUL ZA DOJENČKE IN MAJHNE OTROKE, PRIPRAVLJENIH PO NAVODILIH PROIZVAJALCA Vrednosti, določene v Prilogi, se nanašajo na končno pripravljeni obrok, ki se kot
Microsoft PowerPoint - FK3Anatgonist5HT2c.ppt [Samo za branje] [Združljivostni način]
![Microsoft PowerPoint - FK3Anatgonist5HT2c.ppt [Samo za branje] [Združljivostni način] Microsoft PowerPoint - FK3Anatgonist5HT2c.ppt [Samo za branje] [Združljivostni način]](/thumbs/101/152002466.jpg) Iskanje idealnega anksiolitika Iskanje = načrtovanje, sineza in vrednotenje Iskanje idealnega anksiolitika Kaj je idealni anksiolitik? Idealni anksiolitik: - ni sedativ, - per os uporabna učinkovina -
Iskanje idealnega anksiolitika Iskanje = načrtovanje, sineza in vrednotenje Iskanje idealnega anksiolitika Kaj je idealni anksiolitik? Idealni anksiolitik: - ni sedativ, - per os uporabna učinkovina -
Izpit kemiki 23
 Izpit kemiki 23.4.1992 1.) Skiciraj strukture skupin NO 2+, NO 2-, NO 2. Pripiši sledeče kote O-N-O in razdalje N-O posamezne strukture: koti: 115,4, 180 in 134,3 razdalje: 1,20, 1,15 in 1,24Å 2.) Pri
Izpit kemiki 23.4.1992 1.) Skiciraj strukture skupin NO 2+, NO 2-, NO 2. Pripiši sledeče kote O-N-O in razdalje N-O posamezne strukture: koti: 115,4, 180 in 134,3 razdalje: 1,20, 1,15 in 1,24Å 2.) Pri
Halogenske žarnice (Seminarska) Predmet: Inštalacije HALOGENSKA ŽARNICA
 Halogenske žarnice (Seminarska) Predmet: Inštalacije HALOGENSKA ŽARNICA Je žarnica z nitko iz volframa, okoli katere je atmosfera - prostor, ki vsebuje poleg argona in kriptona doloceno razmerje halogena
Halogenske žarnice (Seminarska) Predmet: Inštalacije HALOGENSKA ŽARNICA Je žarnica z nitko iz volframa, okoli katere je atmosfera - prostor, ki vsebuje poleg argona in kriptona doloceno razmerje halogena
Microsoft PowerPoint - ep-vaja-02-web.pptx
 Goriva, zrak, dimni plini gorivo trdno, kapljevito: C, H, S, O, N, H 2 O, pepel plinasto: H 2, C x H y, CO 2, N 2,... + zrak N 2, O 2, (H 2 O, CO 2, Ar,...) dimni plini N 2, O 2, H 2 O, CO 2, SO 2 + toplota
Goriva, zrak, dimni plini gorivo trdno, kapljevito: C, H, S, O, N, H 2 O, pepel plinasto: H 2, C x H y, CO 2, N 2,... + zrak N 2, O 2, (H 2 O, CO 2, Ar,...) dimni plini N 2, O 2, H 2 O, CO 2, SO 2 + toplota
dr. Andreja Šarlah Teorijska fizika II (FMF, Pedagoška fizika, 2010/11) kolokviji in izpiti Vsebina Kvantna mehanika 2 1. kolokvij 2 2. kolokvij 4 1.
 dr. Andreja Šarlah Teorijska fizika II (FMF, Pedagoška fizika, 2010/11) kolokviji in izpiti Vsebina Kvantna mehanika 2 1. kolokvij 2 2. kolokvij 4 1. izpit 5 2. izpit 6 3. izpit (2014) 7 Termodinamika
dr. Andreja Šarlah Teorijska fizika II (FMF, Pedagoška fizika, 2010/11) kolokviji in izpiti Vsebina Kvantna mehanika 2 1. kolokvij 2 2. kolokvij 4 1. izpit 5 2. izpit 6 3. izpit (2014) 7 Termodinamika
PREPREČEVANJE DEHIDRACIJE Datum: Avtor: Klemen Vidmar Razred: 1.A Mentor: prof. Klemen Gutman Prof. Helena Črne Hladnik
 PREPREČEVANJE DEHIDRACIJE Datum: 6.6.13 Avtor: Klemen Vidmar Razred: 1.A Mentor: prof. Klemen Gutman Prof. Helena Črne Hladnik Kazalo 1. Uvod...3 2. Fizikalne in kemijske lastnosti vode (vodikove vezi)....3,4
PREPREČEVANJE DEHIDRACIJE Datum: 6.6.13 Avtor: Klemen Vidmar Razred: 1.A Mentor: prof. Klemen Gutman Prof. Helena Črne Hladnik Kazalo 1. Uvod...3 2. Fizikalne in kemijske lastnosti vode (vodikove vezi)....3,4
Gorivna celica
 Laboratorij za termoenergetiko Delovanje gorivnih celic Najbolj uveljavljeni tipi gorivnih celic Obstaja veliko različnih vrst gorivnih celic, najpogosteje se jih razvršča glede na vrsto elektrolita Obratovalna
Laboratorij za termoenergetiko Delovanje gorivnih celic Najbolj uveljavljeni tipi gorivnih celic Obstaja veliko različnih vrst gorivnih celic, najpogosteje se jih razvršča glede na vrsto elektrolita Obratovalna
Z ionskimi reakcijami v mavrični svet kemije Zbornik poskusov s tekmovanja iz kemijskih poskusov za osnovne šole Ljubljana,
 Z ionskimi reakcijami v mavrični svet kemije Zbornik poskusov s tekmovanja iz kemijskih poskusov za osnovne šole Ljubljana, 27. 11. 2018 Uredila, priredila in strokovno pregledala: mag. Mojca Orel, Gimnazija
Z ionskimi reakcijami v mavrični svet kemije Zbornik poskusov s tekmovanja iz kemijskih poskusov za osnovne šole Ljubljana, 27. 11. 2018 Uredila, priredila in strokovno pregledala: mag. Mojca Orel, Gimnazija
Tekmovanje iz naravoslovja Državno tekmovanje 25. januar 2014 Čas reševanja: 120 minut. Dovoljeni pripomočki: računalo, ravnilo, kotomer, šestilo, kem
 Tekmovanje iz naravoslovja Državno tekmovanje. januar 0 Čas reševanja: 0 minut. Dovoljeni pripomočki: računalo, ravnilo, kotomer, šestilo, kemični svinčnik, svinčnik, radirka. Periodni sistem je na zadnji
Tekmovanje iz naravoslovja Državno tekmovanje. januar 0 Čas reševanja: 0 minut. Dovoljeni pripomočki: računalo, ravnilo, kotomer, šestilo, kemični svinčnik, svinčnik, radirka. Periodni sistem je na zadnji
Strokovni izobraževalni center Ljubljana, Srednja poklicna in strokovna šola Bežigrad PRIPRAVE NA PISNI DEL IZPITA IZ MATEMATIKE 2. letnik nižjega pok
 Strokovni izobraževalni center Ljubljana, Srednja poklicna in strokovna šola Bežigrad PRIPRAVE NA PISNI DEL IZPITA IZ MATEMATIKE 2. letnik nižjega poklicnega izobraževanja NAVODILA: Izpit iz matematike
Strokovni izobraževalni center Ljubljana, Srednja poklicna in strokovna šola Bežigrad PRIPRAVE NA PISNI DEL IZPITA IZ MATEMATIKE 2. letnik nižjega poklicnega izobraževanja NAVODILA: Izpit iz matematike
1
 Stran 1 od 5 1. IDENTIFIKACIJA SNOVI ALI PRIPRAVKA IN PODATKI O DOBAVITELJU Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka: Dodatek za injekcijsko maso. INJEKTIN F3 Proizvajalec: TKK Proizvodnja
Stran 1 od 5 1. IDENTIFIKACIJA SNOVI ALI PRIPRAVKA IN PODATKI O DOBAVITELJU Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka: Dodatek za injekcijsko maso. INJEKTIN F3 Proizvajalec: TKK Proizvodnja
Dinamika požara v prostoru 21. predavanje Vsebina gorenje v prostoru in na prostem dinamika gorenja v prostoru faze, splošno kvantitativno T
 Dinamika požara v prostoru 21. predavanje Vsebina gorenje v prostoru in na prostem dinamika gorenja v prostoru faze, splošno kvantitativno T pred požarnim preskokom Q FO za požarni preskok polnorazviti
Dinamika požara v prostoru 21. predavanje Vsebina gorenje v prostoru in na prostem dinamika gorenja v prostoru faze, splošno kvantitativno T pred požarnim preskokom Q FO za požarni preskok polnorazviti
Diapozitiv 1
 IDENTIFIKACIJE NPS primeri iz prakse in sodelovanje različnih deležnikov Mojca Janežič E-Mail: mojca.janezic@policija.si MNZ GPU, National Forensic Laboratory, Vodovodna 95, 1000 Ljubljana, Slovenia 1
IDENTIFIKACIJE NPS primeri iz prakse in sodelovanje različnih deležnikov Mojca Janežič E-Mail: mojca.janezic@policija.si MNZ GPU, National Forensic Laboratory, Vodovodna 95, 1000 Ljubljana, Slovenia 1
LaTeX slides
 Statistični modeli - interakcija - Milena Kovač 23. november 2007 Biometrija 2007/08 1 Število živorojenih pujskov Biometrija 2007/08 2 Sestavimo model! Vplivi: leto, farma Odvisna spremenljivka: število
Statistični modeli - interakcija - Milena Kovač 23. november 2007 Biometrija 2007/08 1 Število živorojenih pujskov Biometrija 2007/08 2 Sestavimo model! Vplivi: leto, farma Odvisna spremenljivka: število
Varnostni list ZP
 1/1 1. IDENTIFIKACIJA SNOVI IN DRUŽBE 1.1. Identifikacija snovi ZEMELJSKI PLIN 1.2. Uporaba snovi Snov se uporablja kot gorivo v industriji in široki potrošnji. Lahko se uporablja tudi kot surovina za
1/1 1. IDENTIFIKACIJA SNOVI IN DRUŽBE 1.1. Identifikacija snovi ZEMELJSKI PLIN 1.2. Uporaba snovi Snov se uporablja kot gorivo v industriji in široki potrošnji. Lahko se uporablja tudi kot surovina za
resitve.dvi
 FAKULTETA ZA STROJNISTVO Matematika Pisni izpit. junij 22 Ime in priimek Vpisna st Navodila Pazljivo preberite besedilo naloge, preden se lotite resevanja. Veljale bodo samo resitve na papirju, kjer so
FAKULTETA ZA STROJNISTVO Matematika Pisni izpit. junij 22 Ime in priimek Vpisna st Navodila Pazljivo preberite besedilo naloge, preden se lotite resevanja. Veljale bodo samo resitve na papirju, kjer so
LABORATORIJSKE VAJE IZ FIZIKE
 UVOD LABORATORIJSKE VAJE IZ FIZIKE V tem šolskem letu ste se odločili za fiziko kot izbirni predmet. Laboratorijske vaje boste opravljali med poukom od začetka oktobra do konca aprila. Zunanji kandidati
UVOD LABORATORIJSKE VAJE IZ FIZIKE V tem šolskem letu ste se odločili za fiziko kot izbirni predmet. Laboratorijske vaje boste opravljali med poukom od začetka oktobra do konca aprila. Zunanji kandidati
Namesto (x,y)R uporabljamo xRy
 RELACIJE Namesto (x,y) R uporabljamo xry Def.: Naj bo R AxA D R = { x; y A: xry } je domena ali definicijsko obmocje relacije R Z R = { y; x A: xry } je zaloga vrednosti relacije R Za zgled od zadnjič:
RELACIJE Namesto (x,y) R uporabljamo xry Def.: Naj bo R AxA D R = { x; y A: xry } je domena ali definicijsko obmocje relacije R Z R = { y; x A: xry } je zaloga vrednosti relacije R Za zgled od zadnjič:
Microsoft Word - P-55R EKO PUFER-R za rotacije z manj alkohola.doc
 VARNOSTNI LIST Stran 1 od 6 Datum izdaje: 7. 2. 2002 Ime izdelka: P 55R EKO PUFER-R za rotacije z manj alkohola Datum revidirane revizije: 28. 5. 2008 Štev. revidirane revizije: 4 1. Identifikacija snovi
VARNOSTNI LIST Stran 1 od 6 Datum izdaje: 7. 2. 2002 Ime izdelka: P 55R EKO PUFER-R za rotacije z manj alkohola Datum revidirane revizije: 28. 5. 2008 Štev. revidirane revizije: 4 1. Identifikacija snovi
Univerza v Mariboru Fakulteta za naravoslovje in matematiko Oddelek za matematiko in računalništvo Enopredmetna matematika IZPIT IZ VERJETNOSTI IN STA
 Enopredmetna matematika IN STATISTIKE Maribor, 31. 01. 2012 1. Na voljo imamo kovanca tipa K 1 in K 2, katerih verjetnost, da pade grb, je p 1 in p 2. (a) Istočasno vržemo oba kovanca. Verjetnost, da je
Enopredmetna matematika IN STATISTIKE Maribor, 31. 01. 2012 1. Na voljo imamo kovanca tipa K 1 in K 2, katerih verjetnost, da pade grb, je p 1 in p 2. (a) Istočasno vržemo oba kovanca. Verjetnost, da je
Osnove gastronomije PREBAVA MAKROHRANIL IN Vpliv senzoričnih lastnosti na prebavo Barbara HERLAH, univ. dipl. inž. živ. teh.
 Osnove gastronomije PREBAVA MAKROHRANIL IN Vpliv senzoričnih lastnosti na prebavo Barbara HERLAH, univ. dipl. inž. živ. teh. PREBAVA (DIGESTIJA) IN VSRKAVANJE (ABSORPCIJA) V PREBAVILIH OH, B in M so uporabni
Osnove gastronomije PREBAVA MAKROHRANIL IN Vpliv senzoričnih lastnosti na prebavo Barbara HERLAH, univ. dipl. inž. živ. teh. PREBAVA (DIGESTIJA) IN VSRKAVANJE (ABSORPCIJA) V PREBAVILIH OH, B in M so uporabni
PRILOGA I PARAMETRI IN MEJNE VREDNOSTI PARAMETROV Splošne zahteve za pitno vodo DEL A Mikrobiološki parametri Parameter Mejna vrednost parametra (štev
 PRILOGA I PARAMETRI IN MEJNE VREDNOSTI PARAMETROV Splošne zahteve za pitno vodo DEL A Mikrobiološki parametri (število/100 ml) Escherichia coli (E. coli) 0 Enterokoki 0 Zahteve za vodo, namenjeno za pakiranje:
PRILOGA I PARAMETRI IN MEJNE VREDNOSTI PARAMETROV Splošne zahteve za pitno vodo DEL A Mikrobiološki parametri (število/100 ml) Escherichia coli (E. coli) 0 Enterokoki 0 Zahteve za vodo, namenjeno za pakiranje:
Slide 1
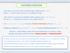 Vsak vektor na premici skozi izhodišče lahko zapišemo kot kjer je v smerni vektor premice in a poljubno število. r a v Vsak vektor na ravnini skozi izhodišče lahko zapišemo kot kjer sta v, v vektorja na
Vsak vektor na premici skozi izhodišče lahko zapišemo kot kjer je v smerni vektor premice in a poljubno število. r a v Vsak vektor na ravnini skozi izhodišče lahko zapišemo kot kjer sta v, v vektorja na
Microsoft Word - Ozon_clanek_2012.doc
 OZON NAŠ ZAŠČITNIK IN SOVRAŽNIK Kaj je ozon Ozon (O 3 ) je plin, katerega molekula je sestavljena iz treh atomov kisika. Pri standardnih pogojih (temperatura 0 C, tlak 1013 hpa) je bledo modre barve. Ozon
OZON NAŠ ZAŠČITNIK IN SOVRAŽNIK Kaj je ozon Ozon (O 3 ) je plin, katerega molekula je sestavljena iz treh atomov kisika. Pri standardnih pogojih (temperatura 0 C, tlak 1013 hpa) je bledo modre barve. Ozon
Microsoft Word - PARKETOLIT 1554A SL.doc
 Datum zadnje revidirane izdaje: 14.01.2013 Zamenjuje izdajo: / VARNOSTNI LIST 1. IDENTIFIKACIJA SNOVI / PRIPRAVKA IN DRUŽBE / PODJETJA: Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka:
Datum zadnje revidirane izdaje: 14.01.2013 Zamenjuje izdajo: / VARNOSTNI LIST 1. IDENTIFIKACIJA SNOVI / PRIPRAVKA IN DRUŽBE / PODJETJA: Identifikacija snovi ali pripravka: Uporaba snovi ali pripravka:
60 Uradni list Evropske unije SL 03/Zv R2316 L 289/4 URADNI LIST EVROPSKIH SKUPNOSTI UREDBA KOMISIJE (ES) št. 2316/98 z dne 26. ok
 60 SL 03/Zv. 24 318R2316 L 28/4 URADNI LIST EVRPSKIH SKUPNSTI 28.10.18 UREDBA KMISIJE (ES) št. 2316/8 z dne 26. oktobra 18 o dovolitvi novih dodatkov in spremembi pogojev za dovolitev več dodatkov, ki
60 SL 03/Zv. 24 318R2316 L 28/4 URADNI LIST EVRPSKIH SKUPNSTI 28.10.18 UREDBA KMISIJE (ES) št. 2316/8 z dne 26. oktobra 18 o dovolitvi novih dodatkov in spremembi pogojev za dovolitev več dodatkov, ki
Microsoft Word - Analiza rezultatov NPZ matematika 2018.docx
 Analiza dosežkov pri predmetu matematika za NPZ 28 6. razred NPZ matematika 28 Dosežek šole Povprečno število točk v % Državno povprečje Povprečno število točk v % Odstopanje v % 49,55 52,52 2,97 Povprečni
Analiza dosežkov pri predmetu matematika za NPZ 28 6. razred NPZ matematika 28 Dosežek šole Povprečno število točk v % Državno povprečje Povprečno število točk v % Odstopanje v % 49,55 52,52 2,97 Povprečni
Microsoft Word - P-55 EKO PUFER z manj alkohola.doc
 VARNOSTNI LIST Stran 1 od 6 Datum izdaje: 3. 5. 2000 Datum revidirane revizije: 28. 5. 2008 Štev. revidirane revizije: 6 1. Identifikacija snovi / pripravka in podatki o dobavitelju: Identifikacija snovi
VARNOSTNI LIST Stran 1 od 6 Datum izdaje: 3. 5. 2000 Datum revidirane revizije: 28. 5. 2008 Štev. revidirane revizije: 6 1. Identifikacija snovi / pripravka in podatki o dobavitelju: Identifikacija snovi
Microsoft Word - Litijev karbonat.doc
 Varnostni list Datum izdaje: 04.11.2003 Nadomesti izdajo 27.04.2002 1. Identifikacija snovi/pripravka in podatki o dobavitelju Identifikacija snovi ali pripravka Trgovsko ime: Uporaba snovi/pripravka:
Varnostni list Datum izdaje: 04.11.2003 Nadomesti izdajo 27.04.2002 1. Identifikacija snovi/pripravka in podatki o dobavitelju Identifikacija snovi ali pripravka Trgovsko ime: Uporaba snovi/pripravka:
Ime in priimek: Vpisna št: FAKULTETA ZA MATEMATIKO IN FIZIKO Oddelek za matematiko Verjetnost Pisni izpit 5. februar 2018 Navodila Pazljivo preberite
 Ime in priimek: Vpisna št: FAKULTETA ZA MATEMATIKO IN FIZIKO Oddelek za matematiko Verjetnost Pisni izpit 5 februar 018 Navodila Pazljivo preberite besedilo naloge, preden se lotite reševanja Nalog je
Ime in priimek: Vpisna št: FAKULTETA ZA MATEMATIKO IN FIZIKO Oddelek za matematiko Verjetnost Pisni izpit 5 februar 018 Navodila Pazljivo preberite besedilo naloge, preden se lotite reševanja Nalog je
Microsoft Word - M docx
 Državni izpitni center *M1180314* SPOMLADANSKI IZPITNI ROK Izpitna pola Modul gradbeništvo NAVODILA ZA OCENJEVANJE Četrtek, 14. junij 01 SPLOŠNA MATURA RIC 01 M11-803-1-4 IZPITNA POLA Modul gradbeništvo
Državni izpitni center *M1180314* SPOMLADANSKI IZPITNI ROK Izpitna pola Modul gradbeništvo NAVODILA ZA OCENJEVANJE Četrtek, 14. junij 01 SPLOŠNA MATURA RIC 01 M11-803-1-4 IZPITNA POLA Modul gradbeništvo
ELEKTRIČNI NIHAJNI KROG TEORIJA Električni nihajni krog je električno vezje, ki služi za generacijo visokofrekvenče izmenične napetosti. V osnovi je "
 ELEKTRIČNI NIHAJNI KROG TEORIJA Električni nihajni krog je električno vezje, ki služi za generacijo visokofrekvenče izmenične napetosti. V osnovi je "električno" nihalo, sestavljeno iz vzporedne vezave
ELEKTRIČNI NIHAJNI KROG TEORIJA Električni nihajni krog je električno vezje, ki služi za generacijo visokofrekvenče izmenične napetosti. V osnovi je "električno" nihalo, sestavljeno iz vzporedne vezave
1
 1 KAZALO Kazalo 2 Ogled Toplarne Moste 3 Zgodovina 3 Splošno 4 O tovarni 5 Okolje 6 2 Ogled Toplarne Moste V ponedeljek ob 9.20 uri smo se dijaki in profesorji zbrali pred šolo ter se nato odpeljali do
1 KAZALO Kazalo 2 Ogled Toplarne Moste 3 Zgodovina 3 Splošno 4 O tovarni 5 Okolje 6 2 Ogled Toplarne Moste V ponedeljek ob 9.20 uri smo se dijaki in profesorji zbrali pred šolo ter se nato odpeljali do
2. izbirni test za MMO 2017 Ljubljana, 17. februar Naj bosta k 1 in k 2 dve krožnici s središčema O 1 in O 2, ki se sekata v dveh točkah, ter
 2. izbirni test za MMO 2017 Ljubljana, 17. februar 2017 1. Naj bosta k 1 in k 2 dve krožnici s središčema O 1 in O 2, ki se sekata v dveh točkah, ter naj bo A eno od njunih presečišč. Ena od njunih skupnih
2. izbirni test za MMO 2017 Ljubljana, 17. februar 2017 1. Naj bosta k 1 in k 2 dve krožnici s središčema O 1 in O 2, ki se sekata v dveh točkah, ter naj bo A eno od njunih presečišč. Ena od njunih skupnih
Microsoft Word - Conditioner for Leather 86 SDS SVN V2.doc
 Varnostni List BALZAM ZA USNJE ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: BALZAM ZA USNJE Koda izdelka: 86 1.2. Pomembne identificirane uporabe snovi ali zmesi
Varnostni List BALZAM ZA USNJE ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: BALZAM ZA USNJE Koda izdelka: 86 1.2. Pomembne identificirane uporabe snovi ali zmesi
Identification Label TRENDS IN INTERNATIONAL MATHEMATICS AND SCIENCE STUDY Mednarodna raziskava trendov znanja matematike in naravoslovja Vprašalnik z
 Identification Label TRENDS IN INTERNTIONL MTHEMTICS ND SCIENCE STUDY Mednarodna raziskava trendov znanja matematike in naravoslovja Vprašalnik za učiteljice in učitelje naravoslovnih predmetov 8. razred
Identification Label TRENDS IN INTERNTIONL MTHEMTICS ND SCIENCE STUDY Mednarodna raziskava trendov znanja matematike in naravoslovja Vprašalnik za učiteljice in učitelje naravoslovnih predmetov 8. razred
B 200 S
 1. Identifikacija zmesi in družbe/podjetja 1.1. Identifikator izdelka 1.2. Pomembne identificirane uporabe zmesi in odsvetovane uporabe Izpiralno sredstvo za profesionalno, strojno uporabo 1.3. Podrobnosti
1. Identifikacija zmesi in družbe/podjetja 1.1. Identifikator izdelka 1.2. Pomembne identificirane uporabe zmesi in odsvetovane uporabe Izpiralno sredstvo za profesionalno, strojno uporabo 1.3. Podrobnosti
VARNOSTNI LIST
 MEGLIO WC DEO Lavanda Varnostni list 1. IDENTIFIKACIJA SNOVI/PRIPRAVKA IN PODATKI O DOBAVITELJU 1.1. Identifikacija snovi ali pripravka: MEGLIO WC DEO Lavanda. 1.2. Podatki o dobavitelju: ARONA TRGOVINA
MEGLIO WC DEO Lavanda Varnostni list 1. IDENTIFIKACIJA SNOVI/PRIPRAVKA IN PODATKI O DOBAVITELJU 1.1. Identifikacija snovi ali pripravka: MEGLIO WC DEO Lavanda. 1.2. Podatki o dobavitelju: ARONA TRGOVINA
POŽAR IN NEVARNE SNOVI
 TEČAJ ZA VODJE ENOTE POŽAR IN NEVARNE SNOVI Avtor: dr. Matija Tomšič, GČ Gradivo dopolnil: Vinko Zobec, VGČ II. st. april 2015 Zakaj v sodobnem gasilstvu enostavno ne gre brez kemije? Gorenje samo je kemijska
TEČAJ ZA VODJE ENOTE POŽAR IN NEVARNE SNOVI Avtor: dr. Matija Tomšič, GČ Gradivo dopolnil: Vinko Zobec, VGČ II. st. april 2015 Zakaj v sodobnem gasilstvu enostavno ne gre brez kemije? Gorenje samo je kemijska
RAČUNALNIŠKA ORODJA V MATEMATIKI
 DEFINICIJA V PARAVOKOTNEM TRIKOTNIKU DEFINICIJA NA ENOTSKI KROŢNICI GRAFI IN LASTNOSTI SINUSA IN KOSINUSA POMEMBNEJŠE FORMULE Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z
DEFINICIJA V PARAVOKOTNEM TRIKOTNIKU DEFINICIJA NA ENOTSKI KROŢNICI GRAFI IN LASTNOSTI SINUSA IN KOSINUSA POMEMBNEJŠE FORMULE Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z
Slide 1
 NAPREDNA OKSIDACIJA IN KAVITACIJA V POSTOPKIH PRIPRAVE PITNE VODE Matej Čehovin, mladi raziskovalec Univerza v Ljubljani, Fakulteta za gradbeništvo in geodezijo, Inštitut za zdravstveno hidrotehniko; MAK
NAPREDNA OKSIDACIJA IN KAVITACIJA V POSTOPKIH PRIPRAVE PITNE VODE Matej Čehovin, mladi raziskovalec Univerza v Ljubljani, Fakulteta za gradbeništvo in geodezijo, Inštitut za zdravstveno hidrotehniko; MAK
Microsoft Word - M docx
 Državni izpitni center *M77* SPOMLADANSK ZPTN OK NAVODLA ZA OCENJEVANJE Petek, 7. junij 0 SPLOŠNA MATA C 0 M-77-- ZPTNA POLA ' ' QQ QQ ' ' Q QQ Q 0 5 0 5 C Zapisan izraz za naboj... točka zračunan naboj...
Državni izpitni center *M77* SPOMLADANSK ZPTN OK NAVODLA ZA OCENJEVANJE Petek, 7. junij 0 SPLOŠNA MATA C 0 M-77-- ZPTNA POLA ' ' QQ QQ ' ' Q QQ Q 0 5 0 5 C Zapisan izraz za naboj... točka zračunan naboj...
Microsoft Word - M docx
 Državni izpitni center *M1380314* JESENSKI IZPITNI ROK Izpitna pola Modul gradbeništvo NAVODILA ZA OCENJEVANJE Sreda, 8. avgust 013 SPLOŠNA MATURA RIC 013 M13-803-1-4 IZPITNA POLA Modul gradbeništvo 1.
Državni izpitni center *M1380314* JESENSKI IZPITNI ROK Izpitna pola Modul gradbeništvo NAVODILA ZA OCENJEVANJE Sreda, 8. avgust 013 SPLOŠNA MATURA RIC 013 M13-803-1-4 IZPITNA POLA Modul gradbeništvo 1.
(Igor Pravst [Združljivostni način])
![(Igor Pravst [Združljivostni način]) (Igor Pravst [Združljivostni način])](/thumbs/102/153614116.jpg) Kongresni center Brdo, 17. oktober 2017 2. nacionalna konferenca o prehrani in telesni dejavnosti za zdravje NACIONALNI PORTAL O HRANI IN PREHRANI WWW.PREHRANA.SI PROF. DR. IGOR PRAVST INŠTITUT ZA NUTRICIONISTIKO
Kongresni center Brdo, 17. oktober 2017 2. nacionalna konferenca o prehrani in telesni dejavnosti za zdravje NACIONALNI PORTAL O HRANI IN PREHRANI WWW.PREHRANA.SI PROF. DR. IGOR PRAVST INŠTITUT ZA NUTRICIONISTIKO
Diapozitiv 1
 ZAHTEVE TENIŠKE IGRE V tej predstavitvi bomo... Analizirali teniško igro z vidika fizioloških procesov Predstavili energijske procese, ki potekajo pri športni aktivnosti Kako nam poznavanje energijskih
ZAHTEVE TENIŠKE IGRE V tej predstavitvi bomo... Analizirali teniško igro z vidika fizioloških procesov Predstavili energijske procese, ki potekajo pri športni aktivnosti Kako nam poznavanje energijskih
VARNOSTNI LIST
 MEGLIO WC DEO Bouquet Varnostni list 1. IDENTIFIKACIJA SNOVI/PRIPRAVKA IN PODATKI O DOBAVITELJU 1.1. Identifikacija snovi ali pripravka: MEGLIO WC DEO Bouquet. 1.2. Podatki o dobavitelju: ARONA TRGOVINA
MEGLIO WC DEO Bouquet Varnostni list 1. IDENTIFIKACIJA SNOVI/PRIPRAVKA IN PODATKI O DOBAVITELJU 1.1. Identifikacija snovi ali pripravka: MEGLIO WC DEO Bouquet. 1.2. Podatki o dobavitelju: ARONA TRGOVINA
UREDBA KOMISIJE (EU) 2018/ z dne 28. septembra o spremembi Priloge II k Uredbi (ES) št. 1333/ Evropskega parlamen
 1.10.2018 L 245/1 II (Nezakonodajni akti) UREDBE UREDBA KOMISIJE (EU) 2018/1461 z dne 28. septembra 2018 o spremembi Priloge II k Uredbi (ES) št. 1333/2008 Evropskega parlamenta in Sveta ter Priloge k
1.10.2018 L 245/1 II (Nezakonodajni akti) UREDBE UREDBA KOMISIJE (EU) 2018/1461 z dne 28. septembra 2018 o spremembi Priloge II k Uredbi (ES) št. 1333/2008 Evropskega parlamenta in Sveta ter Priloge k
ANALITIČNA GEOMETRIJA V RAVNINI
 3. Analitična geometrija v ravnini Osnovna ideja analitične geometrije je v tem, da vaskemu geometrijskemu objektu (točki, premici,...) pridružimo števila oz koordinate, ki ta objekt popolnoma popisujejo.
3. Analitična geometrija v ravnini Osnovna ideja analitične geometrije je v tem, da vaskemu geometrijskemu objektu (točki, premici,...) pridružimo števila oz koordinate, ki ta objekt popolnoma popisujejo.
Prevodnik_v_polju_14_
 14. Prevodnik v električnem polju Vsebina poglavja: prevodnik v zunanjem električnem polju, površina prevodnika je ekvipotencialna ploskev, elektrostatična indukcija (influenca), polje znotraj votline
14. Prevodnik v električnem polju Vsebina poglavja: prevodnik v zunanjem električnem polju, površina prevodnika je ekvipotencialna ploskev, elektrostatična indukcija (influenca), polje znotraj votline
VARNOSTNI LIST v skladu z Uredbo (ES) št. 1907/2006 Datum dopolnjene izdaje Verzija Identifikacija snovi/zmesi in družbe/podjetja 1.
 Datum dopolnjene izdaje 14.01.2011 Verzija 9.7 1. Identifikacija snovi/zmesi in družbe/podjetja 1.1 Identifikator izdelka Kataloška št. Registracijska številka REACH 9974 (glicerol) Registracijska številka
Datum dopolnjene izdaje 14.01.2011 Verzija 9.7 1. Identifikacija snovi/zmesi in družbe/podjetja 1.1 Identifikator izdelka Kataloška št. Registracijska številka REACH 9974 (glicerol) Registracijska številka
KATALOG SREBROVIH SPAJK
 KATALOG SREBROVIH SPAJK UNIVERZALNE SREBROVE SPAJKE BREZ KADMIJA Spajka Sestava % Območje Natezna Standardi Delovna Gostota taljenja trdnost Ag Cu Zn Ostalo temp. g/cm3 EN 17672 DIN 8513 N/mm2 Ag 56Sn
KATALOG SREBROVIH SPAJK UNIVERZALNE SREBROVE SPAJKE BREZ KADMIJA Spajka Sestava % Območje Natezna Standardi Delovna Gostota taljenja trdnost Ag Cu Zn Ostalo temp. g/cm3 EN 17672 DIN 8513 N/mm2 Ag 56Sn
TEČAJ ZA VIŠJEGA GASILCA VIŠJI GASILEC -VG
 TEČAJ ZA VIŠJEGA GASILCA VIŠJI GASILEC -VG POŽAR IN NEVARNE SNOVI Predavatelj: Slavko Tkalec VGČ.II st UČNA VPRAŠANJA Temperature plamenišča,gorišča in vnetišča Parni tlak Agregatno stanje snovi Fizikalno
TEČAJ ZA VIŠJEGA GASILCA VIŠJI GASILEC -VG POŽAR IN NEVARNE SNOVI Predavatelj: Slavko Tkalec VGČ.II st UČNA VPRAŠANJA Temperature plamenišča,gorišča in vnetišča Parni tlak Agregatno stanje snovi Fizikalno
DN080038_plonk plus fizika SS.indd
 razlage I formule I rešeni primeri I namigi I opozorila I tabele Srednješolski Plonk+ Fizika razlage formule rešeni primeri namigi opozorila tabele Avtor: Vasja Kožuh Strokovni pregled: dr. Gorazd Planinšič
razlage I formule I rešeni primeri I namigi I opozorila I tabele Srednješolski Plonk+ Fizika razlage formule rešeni primeri namigi opozorila tabele Avtor: Vasja Kožuh Strokovni pregled: dr. Gorazd Planinšič
7. VAJA A. ENAČBA ZBIRALNE LEČE
 7. VAJA A. ENAČBA ZBIRALNE LEČE 1. UVOD Enačbo leče dobimo navadno s pomočjo geometrijskih konstrukcij. V našem primeru bomo do te enačbe prišli eksperimentalno, z merjenjem razdalj a in b. 2. NALOGA Izračunaj
7. VAJA A. ENAČBA ZBIRALNE LEČE 1. UVOD Enačbo leče dobimo navadno s pomočjo geometrijskih konstrukcij. V našem primeru bomo do te enačbe prišli eksperimentalno, z merjenjem razdalj a in b. 2. NALOGA Izračunaj
Microsoft Word - Down Wash Direct 1K SDS SVN DRAFT.doc
 Varnostni List DOWN WASH DIRECT ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: DOWN WASH DIRECT Koda izdelka: 1.2. Pomembne identificirane uporabe snovi ali zmesi
Varnostni List DOWN WASH DIRECT ODDELEK 1: IDENTIFIKACIJA SNOVI/ZMESI IN DRUŽBE/PODJETJA 1.1. Identifikator izdelka: DOWN WASH DIRECT Koda izdelka: 1.2. Pomembne identificirane uporabe snovi ali zmesi
Predtest iz za 1. kontrolno nalogo- 2K Teme za kontrolno nalogo: Podobni trikotniki. Izreki v pravokotnem trikotniku. Kotne funkcije poljubnega kota.
 Predtest iz za 1. kontrolno nalogo- K Teme za kontrolno nalogo: Podobni trikotniki. Izreki v pravokotnem trikotniku. Kotne funkcije poljubnega kota. Osnovne zveze med funkcijamo istega kota. Uporaba kotnih
Predtest iz za 1. kontrolno nalogo- K Teme za kontrolno nalogo: Podobni trikotniki. Izreki v pravokotnem trikotniku. Kotne funkcije poljubnega kota. Osnovne zveze med funkcijamo istega kota. Uporaba kotnih
Seznam snovi za pripravo pitne vode in seznam postopkov dezinfekcije Snovi za pripravo pitne vode, ki se uporabljajo kot raztopine ali plini Ime snovi
 Seznam snovi za pripravo pitne vode in seznam postopkov dezinfekcije Namen uporabe Zahteve o čistosti ja po 1 aluminijev klorid, brezvodni 7446-70-0 231-208-1 kosmičenje, obarjanje SIST EN 17034 Tabela
Seznam snovi za pripravo pitne vode in seznam postopkov dezinfekcije Namen uporabe Zahteve o čistosti ja po 1 aluminijev klorid, brezvodni 7446-70-0 231-208-1 kosmičenje, obarjanje SIST EN 17034 Tabela
